 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
nmol理想气体由同一始态出发,分别经:(1)等温可逆; (2)绝热可逆两个过程压缩到达相同压力的终态,以H1和H2分别表示(1)和(2)过程终态的焓值,则:()
A.H1>H2
B.H1<H2
C.H1=H2
D.上述三者都对
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.H1>H2
B.H1<H2
C.H1=H2
D.上述三者都对
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“nmol理想气体由同一始态出发,分别经:(1)等温可逆; (…”相关的问题
更多“nmol理想气体由同一始态出发,分别经:(1)等温可逆; (…”相关的问题
A、大于
B、小于
C、等于
物质的量相同的理想气体:O2、He和CO2,从相同始态出发,进行定容吸热过程,如果吸热相同,问温度升高是否相同?压力增加是否相同?
某双原子理想气体从25℃、100kPa、1.00m3始态绝热压缩到500kPa,W=520J,则此过程
(A) 可逆 (B) 不可逆 (C) 达平衡 (D) 无法判定
始态为25℃、100kPa的理想气体发生如下反应(生成的水蒸气近似为理想气体)
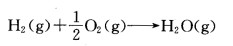 试计算lmol H2与0.5mol O2在不同条件下发生反应的终态温度及过程的W、△U和△H。(1)绝热恒压反应;(2)绝热恒容反应。已知△fHmθ(H2O,g,298.15K)=-241.82kJ.mol-1,Cv,m(H2O,g)=4.5R。
试计算lmol H2与0.5mol O2在不同条件下发生反应的终态温度及过程的W、△U和△H。(1)绝热恒压反应;(2)绝热恒容反应。已知△fHmθ(H2O,g,298.15K)=-241.82kJ.mol-1,Cv,m(H2O,g)=4.5R。
A-3.5kJ
B3.5kJ
C6.0kJ
D-7.6kJ