 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃下,反应平衡时系统中水蒸气压力为 (A) 1.00kPa (B) 10.0kPa (C) 0.100kPa (D) 0.00100kPa
25℃下,反应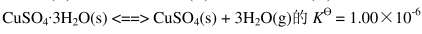 平衡时系统中水蒸气压力为
平衡时系统中水蒸气压力为
(A) 1.00kPa (B) 10.0kPa (C) 0.100kPa (D) 0.00100kPa
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃下,反应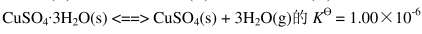 平衡时系统中水蒸气压力为
平衡时系统中水蒸气压力为
(A) 1.00kPa (B) 10.0kPa (C) 0.100kPa (D) 0.00100kPa
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“25℃下,反应平衡时系统中水蒸气压力为 (A) 1.00kP…”相关的问题
更多“25℃下,反应平衡时系统中水蒸气压力为 (A) 1.00kP…”相关的问题
已知乙苯在下列条件下脱氢反应,其平衡转化率为62%,反应条件:
乙苯:水=1:12(mol/mol);
水蒸气过热温度730℃;
乙苯预热温度530℃;
反应压力0.10133MPa。
乙苯脱氢反应式:
C6H5C2H5→C6H5C2H5+H2
试问系统达到平衡时,系统内各组分的分压各为多少?
在容积相等的A、B两密闭容器内,分别通入2molSO2和1molO2使其发生反应

在相同温度下达到平衡。若将A容器保持体积不变,B容器保持压力不变,达平衡时,A容器中SO2的转化率为25%,则B容器中SO2的转化率为
(A) =25% (B) <25% (C) >25% (D) 不能确定
在900K,0.1013MPa下,用甲烷和水蒸气合成CO和H2时,常有副产物CO2存在。系统的反应式为:
 K1=2.053 (1)
K1=2.053 (1)
 K2=3.000 (2)
K2=3.000 (2)
若原料中CH4:H2O=1:1(mol),计算该反应的平衡组成。
对于异构化反应A====B,在400K下可快速建立平衡。在该温度下它们的蒸气压为:

乙烯水合制乙醇反应为 。进料的组成为25%(摩尔)乙烯+75%(摩尔)的水蒸气,试估计125℃时反应物的平衡组成。已知125℃时反应
。进料的组成为25%(摩尔)乙烯+75%(摩尔)的水蒸气,试估计125℃时反应物的平衡组成。已知125℃时反应
在密闭容器中通人体积比为1:3的气体A和气体B,在一定条件下,可逆反应
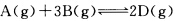 达到平衡时,B的转化率为50%。则同温下容器里反应前的压力和平衡时的压力之比是()。
达到平衡时,B的转化率为50%。则同温下容器里反应前的压力和平衡时的压力之比是()。
A.4:3
B.2:1
C.3:4
D.1:4
组分A按下列反应发生分解:
A====B+C
该反应是在60℃下于液相中进行的。反应的平衡常数为2。组分A、B和C在60℃下的饱和蒸气压分别为607.95kPa、1013.25kPa和810.60kPa。液体A和液体C形成理想溶液。液体B与由(A+C)组成的溶液中互不相溶。假设其汽相为理想气体。试计算该系统在60℃下的汽相组成和平衡压力。
通用气体常数R=1.987cal·mol-1·K-1或8.315J·mol-1·K-1(1cal=4.184J)。
923K等温条件下,于PFR中进行丁烯氧化脱氢生产丁二烯的反应C4H8→C4H6+H2
反应速率方程为:-rA=kpAkmol·m-3·h-1。腺料气为]烯和水蒸气的混合物,其物质的量比为0.5,操作压力为0.1Mpa,反应温度为923K时,k=106.48kmol·m-3·h-1·Mpa-1。试求当丁烯转化率达90%时,空时应为多少秒?
已知反应 在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。
在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。