 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知甲醇CH3OH蒸气与CO在298K时的分别为-161.96和-137.17kJ.mol-1,能否用CO制备甲醇?计算所求反
已知甲醇CH3OH蒸气与CO在298K时的
1.jpg) 分别为-161.96和-137.17kJ.mol-1,能否用CO制备甲醇?计算所求反应的标准平衡常数
分别为-161.96和-137.17kJ.mol-1,能否用CO制备甲醇?计算所求反应的标准平衡常数
2.jpg)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知甲醇CH3OH蒸气与CO在298K时的
1.jpg) 分别为-161.96和-137.17kJ.mol-1,能否用CO制备甲醇?计算所求反应的标准平衡常数
分别为-161.96和-137.17kJ.mol-1,能否用CO制备甲醇?计算所求反应的标准平衡常数
2.jpg)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知甲醇CH3OH蒸气与CO在298K时的分别为-161.9…”相关的问题
更多“已知甲醇CH3OH蒸气与CO在298K时的分别为-161.9…”相关的问题
CO与H2的混合气体在混合催化剂(氧化锌和氧化铬)的条件下进行反应以生产CH3OH。

已知压力平衡常数Kp
平衡常数Kp与温度T的关系式为
lg(Kp×Pa2)=3925/(T/K)-9.841lg(T/K)-0.00347(T/K)+9.8
试计算温度为365℃,压力为300×105Pa,原料气体中CO与H2的比为3:2时,平衡气体中各组分的体积分数。
丙烷C3H8(g)与30%过量空气的混合物在0.1MPa、298K下进入燃烧室,生成物在0.1MPa、920K离开燃烧室。如果已知C的94%生成CO2,其余的C生成CO,试求每kmol燃料的反应热。如果周围环境温度为298K,求该燃烧过程的总熵产。
甲醇(CH3OH)是一种具有高辛烷值并能完全燃烧的“新型燃料”,可以用氢和煤人工制造。 根据: (1)CH3OH(l)+1/2O2(g)=C(石墨)+2H2O(l),△rHΘm=-333.00KJmol-1 (2)C(石墨)+1/2O2(g)=CO(g),△rHΘm=-111.52 kJmol-1 (3)H2(g)+1/2O2(g)——H2O(l),△rHΘm=-285.83 kJmol-1 计算反应(4)2H2(g)+CO(g)=CH3OH(l)的△rHΘm。
5.定温(298K)定压(101325Pa)下,1mol CO燃烧反应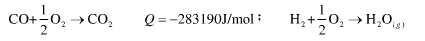 ,放热Q=-283190J/mol,则过程的熵变______J/K,熵流______J/K。已知298K、101325Pa时CO、O2、CO2的摩尔熵分别为197.67J/(mol·K)、205.167J/(mol·K)和213.82J/(mol·K),T0=298K。
,放热Q=-283190J/mol,则过程的熵变______J/K,熵流______J/K。已知298K、101325Pa时CO、O2、CO2的摩尔熵分别为197.67J/(mol·K)、205.167J/(mol·K)和213.82J/(mol·K),T0=298K。
6.Fe(CO)5是一种有毒液体,常作催化剂用于有机合成中,它不溶于水,可溶于CS2。在301K(28℃)将30.0g Fe(CO)5溶于100gCS2中,试求:
(1) 溶液的蒸气压是多少?
(2) 蒸气相中,这两种物质的摩尔分数各是多少?(已知:在301K时Fe(CO)5蒸气压为52.0Pa,CS2的蒸气压为533Pa。)
Fe(CO)5是一种有毒液体,常作催化剂用于有机合成中,它不溶于水,可溶于CS2。在301K(28℃)将30.0g Fe(CO)5溶于100gCS2中,试求:
(1) 溶液的蒸气压是多少?
(2) 蒸气相中,这两种物质的摩尔分数各是多少?(已知:在301K时Fe(CO)5蒸气压为52.0Pa,CS2的蒸气压为533Pa。)
某活性炭吸附甲醇蒸气,在不同压力时的吸附量如下表所示:
 求适用于此实验结果的弗仑因德立希公式。
求适用于此实验结果的弗仑因德立希公式。
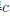 (H2O,1)=-237kJ·mol-1,则反应2H2(g)+O2(g)
(H2O,1)=-237kJ·mol-1,则反应2H2(g)+O2(g) 2H2O(l)在该温度下的
2H2O(l)在该温度下的 为( )。
为( )。A.1.2×1083
B.3.5×1041
C.2.7×10-42
D.7.5×10-84