 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
为了验证某溶液中含有Fe2+而不含有Fe3+,正确的方法是()
A.直接滴加KSCN
B.先滴入KSCN再通入氯气
C.先通入足量氯气再滴入KSCN
D.先加入足量铁粉,充分振荡后再滴加KSCN
 答案
答案
B、先滴入KSCN再通入氯气
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.直接滴加KSCN
B.先滴入KSCN再通入氯气
C.先通入足量氯气再滴入KSCN
D.先加入足量铁粉,充分振荡后再滴加KSCN
 答案
答案
B、先滴入KSCN再通入氯气
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“为了验证某溶液中含有Fe2+而不含有Fe3+,正确的方法是(…”相关的问题
更多“为了验证某溶液中含有Fe2+而不含有Fe3+,正确的方法是(…”相关的问题
(15分)铁及其化合物在国民经济、日常生活中占有非常 重要的地位,了解铁及其化合物的性质和用途非常重要。请回答下列问题: 重要的地位,了解铁及其化合物的性质和用途非常重要。请回答下列问题:(1)铁在自然界中以____态存在,其氧化物呈黑色的是____,呈红褐色的是____(填写化学式)。 (2)铁在纯氧气中燃烧的化学方程式为____。 铁在氯气中反应的产物是____。 (3)要验证一种溶液中是否含有Fe3+、Fe2+,正确的实验方法是____。 A.向甲试管中 B.向乙试管中加入试液,滴入氯水,若氯水褪色,证明一定存在Fe2+。 C.向丙试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中一定存在Fe3+ (4)铁合金有下列数据:
①A、B的作用是____, ②充分加热完全反应后,D装置质量增加0.022g,该样品属于____钢。 ③没有A、B装置,实验结果____(填“偏高”“偏低”“不影响”) |
称取含有Fe3O4,Fe2O3和惰性材料的样品6.000g,用过量的酸性KI水溶液处理,使所有Fe元素转换为Fe2+,稀释至50.00mL,取出10.00mL该溶液,用5.50mL1.00mol·dm-3Na2S2O3滴定生成的I2,这时


配制FeSO4溶液时,一般会加少量金属Fe来防止Fe2+被氧化,其原因是()。
A.加入金属Fe后,氧气不氧化Fe2+了
B.Fe3+可与Fe反应生成Fe2+
C.金属Fe可与溶液中的氢离子反应生成Fe2+
D.金属Fe在溶液中起导电作用
| 为证明化学反应有一定的限度,进行如下探究活动: I.取5m1 0.1mol/L的KI溶液,滴加“滴FeCl3稀溶液(已知:2Fe3++2I-=I2+2Fe2+) Ⅱ.继续加入2ml CCl4振荡 Ⅲ.取萃取后的上层清液,滴加KSCN溶液。 (1)探究活动I的实验现象为_____________________________________________ 探究活动Ⅱ的实验现象为_______________________________________________ (2)探究活动Ⅲ的意图是通过生成血红色的Fe(SCN)3溶液,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈血红色。对此同学们提出了下列两种猜想: 猜想一:Fe3+全部转化为Fe2+ 猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察。 为了验证猜想,查阅资料获得下列信息: 信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大; 信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6](黄色)溶液检验Fe3+的灵敏度比用KSCN更高。 结合新信息。现设计以下实验方案验证猜想: ①请完成下表
Ⅳ.为了测定探究活动I中的FeCl3稀溶液的浓度,现进行以下操作: ①移取25.00mLFeCl3稀溶液至锥形瓶中,加入KSCN溶液作指示剂,再用c mol/L KI标准溶液 滴定,达到滴定终点时的现象是_______________________________________________。 ②重复滴定三次,平均耗用c mol/L KI标准溶液V mL,则FeCl3稀溶液物质的量浓度为________mol/L。 ③若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_______ (填“偏高”或“偏低,,或“不变”)。 |
| 某化学兴趣小组,向HCl 和CuCl2的混合溶液中,加入氢氧化钠溶液,实验结束后, 对所得“蓝色溶液”进一步探究。 【提出问题】 反应后的溶液中含有哪些溶质呢? 【猜想与假设】 甲同学猜想:溶液中溶质为CuCl2、NaCl 。 乙同学猜想:溶液中溶质只含有CuCl2。 【表达与交流】 (1) 甲同学猜想的理由是____________________________________________ ; 【反思与评价】 (2) 请对乙同学的猜想做出评价______________________________________ ; (3) 乙同学为了验证自己的猜想,取少量蓝色溶液于试管中,加入了氢氧化钠溶液,看到蓝 色沉淀,他认为自己的猜想是正确的。请对乙同学的实验设计做出评价______________ ; 【解释与结论】 (4) 若通过实验证明甲同学的猜想是错误的,则蓝色溶液中的溶质的化学式应该是_____ ; 【归纳与总结】 (5) 在探究化学反应后溶液中溶质成分时,需要考虑的是____________________________ 。 |
A.Fe2+/Fe电对的标准电极电势下降
B.Fe2+/Fe电对的标准电极电势上升
C.H+/H2电对的电极电势因(H+)上升而上升
D.H+/H2电对的标准电极电势上升
利用铝热反应焊接钢轨的原理是2Al+Fe2O3 2Fe+ Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褪褐色硬块的组成。 2Fe+ Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褪褐色硬块的组成。样品处理:将褐色硬块处理成粉末状。 (1)研究小组首先取少量粉末加入____溶液中,发现粉末部分溶解,但没有气泡产生,实验结论是:粉末中含有Al2O3而没有Al。 (2)根据以述实验判断该褐色硬块的组成基本确定为Fe、Fe2O3、Al2O3。 提出假设: 假设1:固体粉末中除Al2O3外还有Fe; 假设2:固体粉末中除Al2O3外还有____; 假设3:固体粉末中除Al2O3外还有Fe和Fe2O3。 实验实施: (3)请以上述粉末为样品,验证其组成。限选实验仪器与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、过滤器;20%KSCN、3mol/LNaOH、3mol/LHCl、3mol/LHNO3、3mol/LCuSO4、0.01mol/LKMnO4、蒸馏水。 根据你设计的实验方案,叙述实验操作、预期现象和结论。
|
A.加入H2O2,与钛形成配合物掩蔽 B.加入NaOH使Ti3+生成沉淀而分离
C.以Na2WO4为指示剂,用K2Cr2O7滴定至无色
D.用KMnO4滴定至粉红色 E.控制溶液酸度使Ti3+不干扰
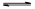 KI3(1)某学习小组对加碘盐进行了如下实验:取一定量加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显示淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。①加KSCN溶液显红色,该试液中含有的物质是________(用离子符号表示);CCl4中显示紫红色的物质是________(用电子式表示)。② 第二份试液中加入足量KI固体后,反应的离子方程式为_______________________。(2)将I2溶于KI溶液,在低温条件下,可制得KI3·H2O。该物质作为食盐加碘剂是否合适?(填“是”或“否”),并说明理由:________________________________。(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失。下列物质中有可能作为稳定剂的是________。
KI3(1)某学习小组对加碘盐进行了如下实验:取一定量加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显示淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。①加KSCN溶液显红色,该试液中含有的物质是________(用离子符号表示);CCl4中显示紫红色的物质是________(用电子式表示)。② 第二份试液中加入足量KI固体后,反应的离子方程式为_______________________。(2)将I2溶于KI溶液,在低温条件下,可制得KI3·H2O。该物质作为食盐加碘剂是否合适?(填“是”或“否”),并说明理由:________________________________。(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失。下列物质中有可能作为稳定剂的是________。A.Na2S2O3
B.AlCl3
C.Na2CO3
D.NaNO2
某矿石样品0.5000克,用重量法测得样品中(Fe2O3+Al2O3)沉淀的总量为0.3630克,将沉淀溶解在酸性溶液中,用重铬酸钾氧化还原滴定法测定铁的含量,将Fe2+还原为Fe2+后,用