 更多“试分析中,哪种离子在水溶液中不能存在?为什么?”相关的问题
更多“试分析中,哪种离子在水溶液中不能存在?为什么?”相关的问题
第1题
钚在水溶液中同时存在_____________________价态离子形式,这一特性在周期表各元素中是唯一的,其
原因是__________________________________________。
点击查看答案
第2题
铀最稳定的价态是________________价,在水溶液中的离子形式为________________,其颜色为________
________;其次较稳定的价态为________________价,水溶液中离子形式为________________。
点击查看答案
第3题
4.将20.0cm30.10mol·dm-3BaCl2水溶液与30.0cm30.10mol·dm-3Na2SO4水溶液混合,试计算溶液中各离子的浓度。
4.将20.0cm30.10mol·dm-3BaCl2水溶液与30.0cm30.10mol·dm-3Na2SO4水溶液混合,试计算溶液中各离子的浓度。
第4题
在“标准”构型搅拌设备中搅拌某种均相水溶液,液体物性数据为:ρ=960kg/m3,μ=0.18P.s。搅拌槽直径=2.
7m,叶轮转速为n=120r/min,试求:全挡板和无挡板条件下的搅拌功率。
点击查看答案
第5题
在水溶液中SO2作为还原剂还原(a)KMnO4溶液到MnSO4;(b)K2Cr2O7的酸性溶液到Cr3+离子;(c)Hg(NO3)2
在水溶液中SO2作为还原剂还原(a)KMnO4溶液到MnSO4;(b)K2Cr2O7的酸性溶液到Cr3+离子;(c)Hg(NO3)2水溶液到金属汞。写出这些反应的方程式。
第6题
若pH=5的HCI溶液用水稀释.1 000倍,HCl浓度为10-8mol.dm-3,此时水溶液中的H+离子浓度也是10-8mol.
.dm-3,且pH=8。这种说法是否正确?为什么?
点击查看答案
第8题
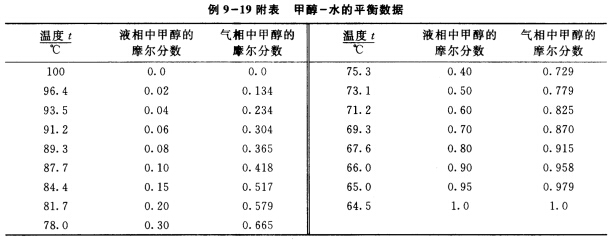
在具有一层理论板和再沸器的精馏装置上回收甲醇水溶液中的甲醇(无回流)。原料液处理量为100kmol/h
在具有一层理论板和再沸器的精馏装置上回收甲醇水溶液中的甲醇(无回流)。原料液处理量为100kmol/h,泡点进料。取样测得馏出液和釜残液的组成分别为0.65和0.1,试求: (1)原料液的组成和甲醇回收率; (2)操作线方程。 甲醇-水的平衡数据示于本题附表中。
第9题
测定水溶液中F-含量时,加入的缓冲试剂的组成为:(1)1 mol.L-的_____________,使溶液保持较大且稳
测定水溶液中F-含量时,加入的缓冲试剂的组成为:(1)1 mol.L-的_____________,使溶液保持较大且稳定的离子强度;(2)0.25 mol.L-的__________和0.75 mol.L-的__________,使溶液pH在5左右;(3)0.001 mol.L-的____________,掩蔽__________等干扰离子。
第11题
在水溶液中,硫化氢还原(a)Fe3+至Fe2+;(b)Br2至Br-;(c)MnO4-至Mn2+;(d)HNO2至NO2。所有反应在适当
在水溶液中,硫化氢还原(a)Fe3+至Fe2+;(b)Br2至Br-;(c)MnO4-至Mn2+;(d)HNO2至NO2。所有反应在适当的条件下,产物皆有硫单质。写出每个反应的离子平衡方程式。

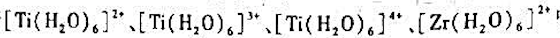 中,哪种离子在水溶液中不能存在?为什么?
中,哪种离子在水溶液中不能存在?为什么?
 如果结果不匹配,请
如果结果不匹配,请 

















