 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有浓度为1.0×10-5mol·L-1的有色物溶液,以2 cm比色皿在最大吸收波长下测得其透光率T=27.5%,换算为
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“有浓度为1.0×10-5mol·L-1的有色物溶液,以2 c…”相关的问题
更多“有浓度为1.0×10-5mol·L-1的有色物溶液,以2 c…”相关的问题
根据A=-lgT=K'c,故K'=2.5×104,今有五个标准溶液,浓度c分别为4.0×10-6mol·L-1、8.0×10-6mol·L-1、1.2×10-5mol·L-1、1.6×10-5mol·L-1、2.0×10-5mol·L-1,绘制以c为横坐标、T为纵坐标的c-T关系曲线图。为什么这样的曲线图不能作定量分析标准曲线?请绘制出可作定量分析的标准曲线。
一标准铜溶液的有色络合物在氯仿中的浓度为6.30×10-5mol·L-1,波长为450nm时,用1cm吸收池测得吸光度A=0.500。某含铜硬币重3.0011g,在25.00mL冷稀盐酸中浸泡1周。经处理显色后,用20.00mL氯仿全部萃取。用1cm吸收池在450nm波长处测得A=0.1250问该硬币溶解损失铜多少克?[M(Cu)=63.55g·mol-1]
A.6.83×10-6molL-1
B.1.4×10-5molL-1
C.9.7×10-7molL-1
D.6.83×10-5mol·L-1
以乙二醇二甲醚为溶剂,以BuLi为引发剂,使苯乙烯聚合,引发剂浓度分别为:4.00×10-4mol·L-1,1.00×10-4mol·L-1,4.45×10-4mol·L-1,2.60×10-5mol·L-1。测得的聚合表观速率常数依次为2.22×103L·mol-1·s-14.24×103L·mol-1·s-1,6.25×103L·mol-1·s-1,8.12×103L·mol-1·s-1。如果电离平衡常数kd=2.4×10-7mol·L-1,用作图法求链增长反应速率常数。
 ,在0.10mol·L-1Ag+溶液中,若产生Ag2CrO4沉淀,
,在0.10mol·L-1Ag+溶液中,若产生Ag2CrO4沉淀, 浓度应至少大于( )
浓度应至少大于( )A.1.1×10-11mol·L-1
B.6.5×10-5mol·L-1
C.0.10mol·L-1
D.1.1×10-10mol·L-1
一级反应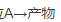 ,初始速率为1.0×10-5mol·dm-3·s-1,3600s时的速率为0.25mol·dm-3·s-1,求:k,t1/2和初始浓度
,初始速率为1.0×10-5mol·dm-3·s-1,3600s时的速率为0.25mol·dm-3·s-1,求:k,t1/2和初始浓度
极谱定量分析的依据id=Kc,适合的浓度测量范围是10-2~10-5mol·L-1,若在很浓的溶液中,则______;若在极稀的溶液中,则产生______。
在0.50mol·L-1H2SO4溶液中电解1.00×10-3mol·L-1ZnSO4溶液,锌是否可在镀锌的铂电极上析出?如果介质c(H+)=1.00×10-5mol·L-1时,锌是否能析出?已知,在锌电极上η(H2)=-0.70V,
某可逆反应 在某温度时的
在某温度时的
在298K时,反应 的各物质起始浓度分别为
的各物质起始浓度分别为
c(
c(
而