 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算1mol H2(g)与0.5molO2(g)结合生成H2O(1)所放出的热量。 (2)计算1kg H2完全燃烧放出的
计算1mol H2(g)与0.5molO2(g)结合生成H2O(1)所放出的热量。 (2)计算1kg H2完全燃烧放出的热量,并以此与同量的煤(设仅含12C)完全燃烧放出的热量作一比较,得出何种结论?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算1mol H2(g)与0.5molO2(g)结合生成H2O(1)所放出的热量。 (2)计算1kg H2完全燃烧放出的热量,并以此与同量的煤(设仅含12C)完全燃烧放出的热量作一比较,得出何种结论?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算1mol H2(g)与0.5molO2(g)结合生成H2…”相关的问题
更多“计算1mol H2(g)与0.5molO2(g)结合生成H2…”相关的问题
煤和由煤与水蒸气反应[C(s)+H2O(g)=H2(g)+CO(g)]而得的水煤气(CO与H2等物质的混合物)都可用做燃料。设煤含碳80%,其余可燃成分忽略不计。试通过计算说明,在实际应用中以水煤气代替煤作燃料的优点。(提示:在任何能量转换过程中,总会有一些能量变成热而扩散到环境中。例如,欲往某体系输入xkJ的能量,实际上提供的热量要远多于该值。)
两种脂肪酸三甘油酯的异构体水解后均得到1mol A(C17H33COOH)和2mol B(C17H35COOH)。化合物B还原后生成正硬脂醇CH3(CH2)16CH2OH。化合物A与1mol H2反应生成B,A发生臭氧化还原水解生成壬醛和9一羰基壬酸O=CH(CH2)7COOH。试推测这两个异构体的结构。
已知Mg(s)→Mg(g) △H1=147 kJ.mol-1 Mg(g)→Mg2+(g)+2e- △H2=2 188 kJ.mol-1 S(s)→S(g) △H3=277 kJ.mol-1 S(g)+2e-→S2-(g) △H4=332 kJ.mol-1 Mg(s)+S(s)→MgS(s) △H5=一347 kJ.mol-1 计算MgS的晶格能U。
在天然气产地,可以用甲烷分解法制备H2。实际生产时是将H2O(g)和O2 (g)同时通入高温反应塔,CH4分别和它们起反应。写出这两个化学反应方程式,分别计算
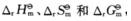 ,并说明通入O2的目的?
,并说明通入O2的目的?
A.∆U
B.∆S体
C.∆A
D.∆G
13.8gO2与______g H2或______LN2(标准状况下)所含有的分子数相同。
下列反应制备的氢气纯度最高的是 ()
A.CO(g)+H2O(g)====CO2(g)+H2(g)
B.Si粉与NaOH溶液反应
C.锌粒与稀盐酸反应
D.25%NaOH溶液电解
甲醇(CH3OH)是一种具有高辛烷值并能完全燃烧的“新型燃料”,可以用氢和煤人工制造。 根据: (1)CH3OH(l)+1/2O2(g)=C(石墨)+2H2O(l),△rHΘm=-333.00KJmol-1 (2)C(石墨)+1/2O2(g)=CO(g),△rHΘm=-111.52 kJmol-1 (3)H2(g)+1/2O2(g)——H2O(l),△rHΘm=-285.83 kJmol-1 计算反应(4)2H2(g)+CO(g)=CH3OH(l)的△rHΘm。