 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知,通过计算判断下列反应能否发生。 3HgS+(1.0mol·dm-3)+8H+(1.0mol·dm-3)3Hg2+(0.1mol·dm-3)+3S↓+2NO(p)
已知,通过计算判断下列反应能否发生。
3HgS+(1.0mol·dm-3)+8H+(1.0mol·dm-3)
 3Hg2+(0.1mol·dm-3)+3S↓+2NO(p)+4H2O
3Hg2+(0.1mol·dm-3)+3S↓+2NO(p)+4H2O
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知,通过计算判断下列反应能否发生。
3HgS+(1.0mol·dm-3)+8H+(1.0mol·dm-3)
 3Hg2+(0.1mol·dm-3)+3S↓+2NO(p)+4H2O
3Hg2+(0.1mol·dm-3)+3S↓+2NO(p)+4H2O
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知,通过计算判断下列反应能否发生。 3HgS+(1.0mo…”相关的问题
更多“已知,通过计算判断下列反应能否发生。 3HgS+(1.0mo…”相关的问题
根据已知数据判断下列反应能否发生:




判断化合物
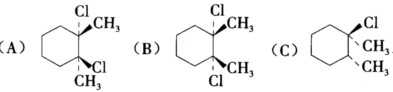 与下列试剂能否发生反应?如能发生,写出反应的主要产物。 (i)NaOH (ii)Zn (iii)H2O (iv)C2H5OH
与下列试剂能否发生反应?如能发生,写出反应的主要产物。 (i)NaOH (ii)Zn (iii)H2O (iv)C2H5OH
已知(a)ADP+Pi→ATP+H2O的△G0=+7.3 kcal.mol-1: (b)PEP+H2O→丙酮酸+Pi的△G0= 一14.8 kcal.mol-1。 判断这两个反应能否自发进行?如果这两个反应耦联起来能自发进行吗?
常温下BBr3是液态的,能否根据已知其△fGΘm(298K)说明反应BBr3(g)=B(s)+3/2Br2(g)在常温下是否可以自发进行?
2NO(g)+O2(g)====2NO2(g)


若


已知下列反应△rHΘm值的正、负,判断反应在高温和低温时的自发状态。 (1)2Fe(S)+3/2O2(g)=Fe2O3(s) △rHΘm<0 (2)2NH3(g)=N2(g)+3H2(g) △rHΘm>0 (3)C2H5OH(1)=C2H5OH(g) △rHΘm>0 (4)2Cl2(g)+7O2(g)=2Cl2O7(l) △rHΘm>0 (5)C2H5OH(l)+2O2(g)=2CO2(g)+3H2O(g) △rHΘm<0
在生命过程中,Fe(Ⅱ/Ⅲ)离子催化·OH生成反应:
催化还原:FeⅡL+H2O2→FeⅢL+·OH+OH-
催化氧化:FeⅢL+生物还原剂→FeⅡL+氧化产物
总反应:生物还原剂+H2O2→·OH+OH-+氧化产物
其中,氧化半反应:H2O2+H++e→·OH+H2O
还原半反应:生物还原剂-ne→氧化产物
因此,Fe(Ⅱ/Ⅲ)配离子催化上述反应的条件是其氧化还原电位处于-0.35~0.32V之间,这样既可以被H2O2氧化,又可以被生物还原剂还原。请计算下列哪种配体可以阻止上述反应发生:(1)EDTA;(2)吡咯二羧酸;(3)柠檬酸;(4)水杨酸;(5)邻菲罗啉。
已知:Fe3++e→Fe2+
配合物稳定常数:
| EDTA(Y4-) | 吡咯二羧酸(Dipic2-) | 柠檬酸(Cit3-) | 水杨酸(Sal-) | 邻菲罗啉(o-Phen) | |
| Fe2+ | lgβ1=14.33 | 1gβ2=10.36 | lgβ1=15.5 | lgβ2=11.25 | lgβ3=21.3 |
| Fe3+ | lgβ1=24.23 | lgβ2=17.13 | lgβ1=25.0 | lgβ3=36.8 | lgβ3=23.5 |
合成CuCl通常采用SO2还原CuSO4的方法,其工艺流程如下:
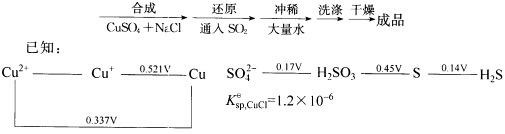 (1)通过计算说明,为什么合成反应中一定要加入NaCl。 (2)为了加快氯化亚铜的合成速度,温度高一点好(70~80℃),还是低一点好(30~40℃)?请提出观点,并加以分析。 (3)写出合成中的总反应(离子方程式),如何判断反应已经完全? (4)合成反应结束后,为什么要迅速洗涤和干燥?
(1)通过计算说明,为什么合成反应中一定要加入NaCl。 (2)为了加快氯化亚铜的合成速度,温度高一点好(70~80℃),还是低一点好(30~40℃)?请提出观点,并加以分析。 (3)写出合成中的总反应(离子方程式),如何判断反应已经完全? (4)合成反应结束后,为什么要迅速洗涤和干燥?
已知反应
式中k1=1×107mol-1·s-1;k-1=1×102mol-1·s-1;k2=3×102mol-1·s-1,计算