 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在铵盐存在下,利用氨水沉淀Fe3+,若按盐浓度固定,增大氨的浓度,Fe(OH)3沉淀对Ca2+、Mg2+、Zn2+、Ni2+等四种离子的吸附量将是()
A、都增加
B、都减少
C、Zn2+、Ni2+增加,而Ca2+、Mg2+减少
D、Ca2+、Mg2+增加,而Zn2+、Ni2+减少
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、都增加
B、都减少
C、Zn2+、Ni2+增加,而Ca2+、Mg2+减少
D、Ca2+、Mg2+增加,而Zn2+、Ni2+减少
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在铵盐存在下,利用氨水沉淀Fe3+,若按盐浓度固定,增大氨的…”相关的问题
更多“在铵盐存在下,利用氨水沉淀Fe3+,若按盐浓度固定,增大氨的…”相关的问题
以氨水沉淀Fe3+时,溶液中含有Ca2+、Zn2+,当固定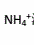 浓度、增大NH3浓度时,______的吸附量增大,______的吸附量减小。
浓度、增大NH3浓度时,______的吸附量增大,______的吸附量减小。
为分析硅酸盐中铁、铝、钛含量,称取试样0.6250g。除去SiO2后,用氨水沉淀铁、铝、钛为氢氧化物沉淀。沉淀灼烧为氧化物后重0.4165g。再将沉淀用K2S2O7熔融,浸取液定容于100mL容量瓶中。移取25.00mL试液通过锌汞还原器,含Fe2+和Ti3+的已还原液用含Fe3+的溶液承接,Fe3+被流入的Ti3+还原为Fe2+。然后用浓度为0.01390mol·L-1的K2Cr2O7标准溶液滴定,用去9.94mL。另取等量试液,用SnCl2将Fe3+还原为Fe2+,再用上述K2Cr2O7标准溶液滴定,用去8.82mL。计算试样中Fe2O3、Al2O3和TiO2的含量。[M(Fe2O3)=159.7g·mol-1,M(TiO2)=79.84g·mol-1,M(Al2O3)=102.0g·mol-1]
某酸性BaCl2溶液中含少量FeCl3杂质。用Ba(OH)2或BaCO3调节溶液的pH,均可把Fe3+沉淀为Fe(OH)3而除去。为什么?利用平衡移动原理进行讨论。
A.利用电解法分离;
B.加入抗坏血酸或盐酸羟胺等还原剂使其还原为Fe2+;
C.加入NaOH使其形成沉淀而除去;
D.加入SCN-使其形成配合物而除去。
在下面的反应中,利用Libido定律预测哪个酸能给出特殊催化或一般催化(亚胺共轭酸的pKa大概在4到5左右):HCl、苦味酸、乙酸、氨水和苯酚。重要的是要记住发生特殊催化或者是一般催化,不仅仅与酸的pKa有关,也与底物的反应性有关。
