 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
证明Wilson方程不能应用表达液液平衡关系(以二元系统为例)。
证明Wilson方程不能应用表达液液平衡关系(以二元系统为例)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
证明Wilson方程不能应用表达液液平衡关系(以二元系统为例)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“证明Wilson方程不能应用表达液液平衡关系(以二元系统为例…”相关的问题
更多“证明Wilson方程不能应用表达液液平衡关系(以二元系统为例…”相关的问题
CH4—H2S混合物的汽液平衡数据回归
题目:利用与天然气膨胀装置设计有关的CH4—H2S混合物的汽液平衡数据。在本例中,部分由Reamen等(1951)测定的P-x-Y数据示于下图3.2,这里应用了回归分析的方法,使Soave-Redlich-Kwong(SRK)方程能更好地对数据进行表达。
| VLE数据(Reamer等1951) | ||||
| pressure(psi) | CH4 | H2S | CH4 | H2S |
| 0.10% 200 300 400 500 600 700 800 1000 1200 1400 1600 | 0.10% 0.005 0.021 0.035 0.049 0.062 0.071 0.09 0.125 0.162 0.205 0.238 | 0 0.995 0.979 0.965 0.951 0.938 0.929 0.91 0.875 0.838 0.795 0.762 | 1% 0.14 0.392 0.513 0.58 0.632 0.655 0.69 0.72 0.727 0.725 0.705 | 0 0.86 0.608 0.487 0.42 0.368 0.345 0.31 0.28 0.273 0.275 0.295 |

二元系统的Wilson模型参数是λ12=1718cal·mol-1和λ21=166.6cal·mol-1,假设气相是理想气体,计算与x1=0.2,T=30℃的液相成平衡的气相组成和总压。已知


110℃时,水(1)-正丁醇(2)液液平衡数据为x'1=0.9788,x"2=0.6759。试计算汽相的组成y及总压p。
已知饱和蒸气压为:
活度系数采用Van Laar方程计算:
其中A、B为活度系数方程参数。
已知50℃,64kPa,丙酮(1)-乙腈(2)系统,求气液平衡时的气、液相分率V,L和组成x1,y1。已知纯组分的蒸气压
AiBiCi
NN(1) 14.37284 2787.498 229.664
乙腈(2) 14.88567 3413.099 250.523
A.错误
B.正确
若二元气液平衡系统的气相可视作理想气体,试证明(a)p-x1-y1图上的泡点曲线的斜率为;(b)若液相的超额Gibbs函数模型是GE/RT=Bx1x2,则当
时有共沸点存在;且对于
和B<2时,共沸组成是
。
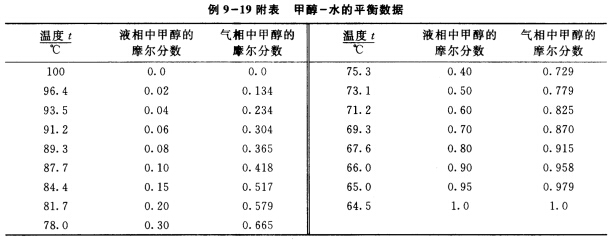
在具有一层理论板和再沸器的精馏装置上回收甲醇水溶液中的甲醇(无回流)。原料液处理量为100kmol/h,泡点进料。取样测得馏出液和釜残液的组成分别为0.65和0.1,试求: (1)原料液的组成和甲醇回收率; (2)操作线方程。 甲醇-水的平衡数据示于本题附表中。
已知化合物A、B属于同系物,其蒸气压如下:
温度/℃ | p_A^S/kPa | p_B^S/kPa |
65.6 | 80.0 | 66.66 |
93.3 | 133.32 | 126.66 |
假设化合物组成理想溶液,计算:79.4℃,xA=0.500时,达到汽液平衡时组分A的气相摩尔分数和系统的总压。已知:Clausius-Clapeyron方程为。