
天津大学20春《无机化学》在线作业2答案试卷(40)
试题 2
[主观题]
BeCl₂和OF₂同为AB₂型分子,它们的中心原子均采取sp杂化的方式成键。()
BeCl₂和OF₂同为AB₂型分子,它们的中心原子均采取sp杂化的方式成键。()
A.正确
B.错误
试题 3
[单选题]
下列陈述中错误的是在一定温度下,将1.00mol的SO₃放在1.00L的密闭容器中,反应2SO₂(g)+O₂(g)=2SO₃(g)达到平衡时,SO₂为0.60mol,则反应的Kc为多少mol/L?()
A.2.8
B.2.2
C.1.5
D.1.9
试题 4
[主观题]
由于Ag⁺与S²⁻之间的相互极化作用比Cu⁺与S²⁻之间的极化作用强,所以Ag₂S比Cu₂S的溶解度小。()
由于Ag⁺与S²⁻之间的相互极化作用比Cu⁺与S²⁻之间的极化作用强,所以Ag₂S比Cu₂S的溶解度小。()
A.正确
B.错误
A.正确
B.错误
试题 8
[主观题]
C和H形成CH₄时,H原子的1s轨道和C原子的3个2p轨道杂化形成4个sp³杂化轨道成键的。()
C和H形成CH₄时,H原子的1s轨道和C原子的3个2p轨道杂化形成4个sp³杂化轨道成键的。()
A.正确
B.错误
A.正确
B.错误
试题 10
[单选题]
以下配合物中心离子的配位数为6,假定它们的浓度均为0.001mol/L,指出下图各溶液导电能力强弱的顺序为()。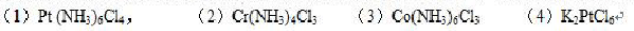
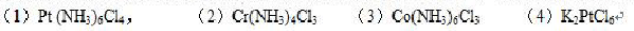
A.(1)>(3)>(4)>(2)
B.(4)>(3)>(1)>(2)
C.(1)>(4)>(3)>(2)
D.(2)>(4)>(3)(>1)
试题 12
[主观题]
某反应的速率方程式是,当A的浓度减少50%时,v降低至原来的1/4,当B的浓度增大至2倍时,v增大1.41
某反应的速率方程式是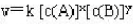 ,当A的浓度减少50%时,v降低至原来的1/4,当B的浓度增大至2倍时,v增大1.41倍,则x=2,y=0.7。()
,当A的浓度减少50%时,v降低至原来的1/4,当B的浓度增大至2倍时,v增大1.41倍,则x=2,y=0.7。()
A.正确
B.错误
某反应的速率方程式是
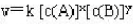 ,当A的浓度减少50%时,v降低至原来的1/4,当B的浓度增大至2倍时,v增大1.41倍,则x=2,y=0.7。()
,当A的浓度减少50%时,v降低至原来的1/4,当B的浓度增大至2倍时,v增大1.41倍,则x=2,y=0.7。()A.正确
B.错误
试题 14
[单选题]
下列分子中,其中心原子采取等性sp²杂化轨道成键的是()。
A.Al₂Cl₆,分子中各原子不在同一平面
B.C₂H₂,直线型分子
C.C₂H₄,分子中各原子均在同一平面
D.NCl₃,原子不在同一平面
试题 15
[主观题]
在N₂的分子轨道能级顺序中,因此N₂参加反应时,首先打开σ键。()
在N₂的分子轨道能级顺序中,因此N₂参加反应时,首先打开σ键。()
在N₂的分子轨道能级顺序中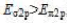 ,因此N₂参加反应时,首先打开σ键。()
,因此N₂参加反应时,首先打开σ键。()
A.正确
B.错误
在N₂的分子轨道能级顺序中
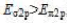 ,因此N₂参加反应时,首先打开σ键。()
,因此N₂参加反应时,首先打开σ键。()A.正确
B.错误
试题 18
[主观题]
当溶液中H⁺离子浓度增大时,的氧化能力增强,的氧化能力不变。()
当溶液中H⁺离子浓度增大时,的氧化能力增强,的氧化能力不变。()
当溶液中H⁺离子浓度增大时,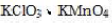 的氧化能力增强,
的氧化能力增强,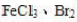 的氧化能力不变。()
的氧化能力不变。()
A.正确
B.错误
当溶液中H⁺离子浓度增大时,
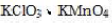 的氧化能力增强,
的氧化能力增强,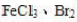 的氧化能力不变。()
的氧化能力不变。()A.正确
B.错误
试题 19
[单选题]
反应PCl₅=PCl₃+Cl₂在200℃达到平衡时,PCl₅有48.5%分解,在300摄氏度有97.4%分解,该反应式是()。
A.放热反应
B.平衡常数为2
C.吸热反应
D.这两个温度下的平衡常数相等
试题 30
[单选题]
在下列分子中,其中心原子采取sp²杂化轨道成键的是()。
A.B₂H₆,分子中各原子不在同一平面
B.HCN,直线型分子
C.C₂H₄,分子中各原子均在同一平面
D.NCl₃,原子不在同一平面
试题 31
[单选题]
已知电极反应Cu²⁺+2e⁻→Cu的标准电极电势为0.342V,则电极反应2Cu²⁺+4e⁻→2Cu的标准电极电势是()。
A.0.684V
B.-0.684V
C.0.342V
D.-0.342V
试题 34
[单选题]
已知反应式CaO(s)+H₂O(l)→Ca(OH)₂(s)在室温下可自发进行,但在高温下不能自发进行,据此可知该反应的()。
A.△rHmθ<0,△rSmθ>0
B.△rHmθ>0,△rSmθ<0
C.△rHmθ<0,△rSmθ<0
D.△rHmθ>0,△rSmθ>0
试题 35
[单选题]
下列说法正确的是()。
A.中心原子中的几个原子轨道杂化时,必形成数目相同的杂化轨道
B.sp²杂化轨道是由某个原子的1s轨道和2p轨道混合形成的
C.原子在基态时没有未成对电子就一定不能形成共价键
D.在CCl₄、CHCl₃和CH₂Cl₂分子中,碳原子都采用sp³杂化,因此这些分子都是呈正四面体形
试题 37
[主观题]
NaF和NaCl均为离子晶体,电荷数相同,但r(F⁻)<r(Cl⁻),晶格能:NaF>NaCl。所以NaF的熔点高于NaCl。()
NaF和NaCl均为离子晶体,电荷数相同,但r(F⁻)<r(Cl⁻),晶格能:NaF>NaCl。所以NaF的熔点高于NaCl。()
A.正确
B.错误
试题 39
[单选题]
某弱碱ROH的相对分子质量为125,在298K时取0.500g溶于50.00ML水中所得溶液PH值是11.3,该弱碱的Kbθ值是()。
A.2.70×10⁻⁵
B.6.00×10⁻⁵
C.5.50×10⁻⁵
D.4.98×10⁻⁵
试题 40
[单选题]
已知反应式中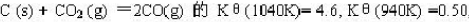 ,下列叙述中不正确的是()。
,下列叙述中不正确的是()。
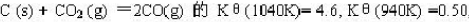 ,下列叙述中不正确的是()。
,下列叙述中不正确的是()。
A.恒温、恒容条件下,压入氖气,化学平衡不移动
B.上述反应为放热反应
C.增大体系的总压,平衡发生移动
D.增大二氧化碳的浓度,平衡向正反应方向移动

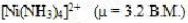
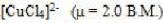
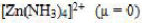
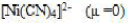







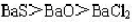
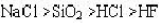
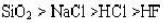
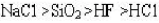
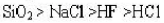
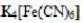
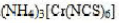
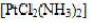
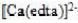
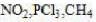
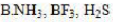
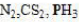
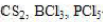
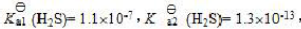 ,那么0.1mol/L的H₂S溶液中,其各物质浓度大小次序正确的是()。
,那么0.1mol/L的H₂S溶液中,其各物质浓度大小次序正确的是()。
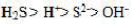
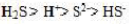
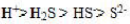
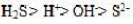
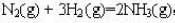 ,保持温度、压力不变,加入稀有气体He,使总体积增加一倍,则()。
,保持温度、压力不变,加入稀有气体He,使总体积增加一倍,则()。



