 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某二级反应,其在不同温度下的反应速率常数如下: T/K 645 675 715 750 k×103/(mol-1·L·mi
某二级反应,其在不同温度下的反应速率常数如下:
T/K 645 675 715 750
k×103/(mol-1·L·min-1) 6.15 22.0 77.5 250
(1)作lnk-1/T图,计算反应活化能Ea;
(2)计算700K时的反应速率常数k。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某二级反应,其在不同温度下的反应速率常数如下:
T/K 645 675 715 750
k×103/(mol-1·L·min-1) 6.15 22.0 77.5 250
(1)作lnk-1/T图,计算反应活化能Ea;
(2)计算700K时的反应速率常数k。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某二级反应,其在不同温度下的反应速率常数如下: T/K 64…”相关的问题
更多“某二级反应,其在不同温度下的反应速率常数如下: T/K 64…”相关的问题
二氧化氮分解为二级反应,不同温度下测得的反应速率常数如下:
T(K) | 592 | 603 | 627 | 651 | 656 |
k,cm3/(mol·s) | 522 | 755 | 1700 | 4020 | 5030 |
计算反应活化能。
反应mA+nB====pC+qD对A是一级反应,对B是二级反应,某温度时,当A和B相等都等于2.0mol·dm-3时,反应速率为0.10mol·dm-3·s-1,则当c(A)=4.0mol·dm-3,c(B)=2.0mol·dm-3,同温下,反应速率常数和反应速率的数值分别为( )和( )。
(A) 0.5 (B) 0.1 (C) 0.2
(D) 0.025 (E) 0.0125
某分解反应在10℃的速率常数为4.5×10-3s-1,活化能为58kJ·mol-1,求在什么温度下,该反应的速率常数为10×10-4s-1?
间歇反应器中反应的实验研究
醋酐稀水溶液的液相水解是两级不可逆反应:
(CH3CO)2O+H2O→2CH3COOH
在15℃下将200L的浓度为2.16×10-4mol/cm3的醋酐溶液加入间歇反应器进行水解。反应混合物的密度假设为常数1.05g/cm3。在不同温度下速率表达式为
T(℃) | 10 | 15 | 25 | 40 |
(-rA)【mol/(cm3·min)】 | 0.0567cA | 0.0806cA | 0.1580cA | 0.380cA |
式中cA为醋酐浓度,以mol/cm3表示。
(1)解释该反应为二级反应,为什么反应速率可以用表中所列方式表示。
(2)倘若在15℃下等温操作,当醋酐的转化率为0.7时,需要多少时间?
(3)确定该反应速率表达式。
某溶液的反应A+B→P,当A和B的起始浓度为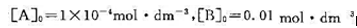 时,实验测得不同温度下吸光度随时间的变化如下表:
时,实验测得不同温度下吸光度随时间的变化如下表:
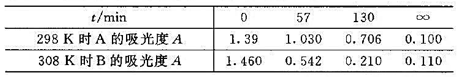
当固定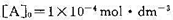 ,改变[B]o时,实验测得在298 K时,t1/2随[B]0的变化如下表:
,改变[B]o时,实验测得在298 K时,t1/2随[B]0的变化如下表:

设速率方程为r=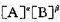 ,试计算α、β、速率常数k和实验活化能
,试计算α、β、速率常数k和实验活化能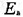 。
。
某二级反应800℃下的速率常数k1=5.0×10-3dm3·mol-1·s-1,活化能Ea=45kJ·mol-1,则875℃下的速率常数k2=______dm3·mol-1·s-1。
元反应2A+B=2C,某浓度下当温度为T时反应速率为v,速率常数为k;当温度为T2时,反应速率为v2,速率常数为k2。若T>T2,则下列关系正确的是( )。
(A) v>v2,k>k2(B) v-v2,k>k2
(C) v<v2,k<k2(D) v>v2,k=k2
A.10mol-1?L?min-1
B.0.1mol-1?L?min-1
C.0.1mol?L-1?min-1
D.10mol?L-1?min-1
温度423K,一级反应A→R在PFR中进行,反应活化能为83.74kJ·mol-1,需反应器体积为Vp。若改用CSTR,其体积为VT,试推导VP和VT的关系。若转化率为60%,欲使VP=VT,则两种反应器内的反应速率常数kT应为kP的多少倍?若CSTR也在等温下操作,则反应温度是多少?
与温度的关系为
k=3.452×10-5exp(-10983/T) [kmol/(s·kg·Pa)]
不同温度下的化学平衡常数值可根据下列近似式估算:
K=3.96×1011exp(-14.520/T) (Pa-1)
反应混合物的平均比热容为2.177kJ/(kg·K),反应热为1.39×105J/mol,催化剂床层的堆密度为1440kg/m3。试计算
(1)催化剂用量;
(2)反应器的轴向温度及转化率分布。