 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
图所示为三端网络,端子用a,d,e标记。已知R=1Ω,C=0.1F,L=0.5H,uab=sin10tV,udc=e-2tV,idc(0)=1A.求t>0时的ubc
图所示为三端网络,端子用a,d,e标记。已知R=1Ω,C=0.1F,L=0.5H,uab=sin10tV,udc=e-2tV,idc(0)=1A.求t>0时的ubc。

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
图所示为三端网络,端子用a,d,e标记。已知R=1Ω,C=0.1F,L=0.5H,uab=sin10tV,udc=e-2tV,idc(0)=1A.求t>0时的ubc。

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“图所示为三端网络,端子用a,d,e标记。已知R=1Ω,C=0…”相关的问题
更多“图所示为三端网络,端子用a,d,e标记。已知R=1Ω,C=0…”相关的问题
F.W.Stahl的实验室做过下列实验。基因型为red-gamA-的噬菌体λ用13C和15N进行密度标记,再与含13C和14N的λred-gainR-混合。用该混合液在下述条件下感染大肠杆菌:抑制DNA的复制;每个细菌感染10个病毒颗粒。所产生的噬菌体在硫酸铯中离心平衡,检测分布在密度梯度中的基因型,可以观察到如图12-3-12所示的全部噬菌体和A+R+重组子的分布图谱。在第二个实验中,两种噬菌体都含有突变,该突变位置是在噬菌体遗传图左端约93%处,该实验结果见图12-3-12B。试解释两个实验结果。

1.jpg) (1)EcoRⅠ到HindⅢ位点间的片段有多大? (2)画出HhaⅠ和Sau3A的酶切位点。 (3)标记有32p的同样DNA片段,用HhaⅠ完全酶切,进行电泳,那么用EB染色或放射自显影,会分别得到什么样的图?
(1)EcoRⅠ到HindⅢ位点间的片段有多大? (2)画出HhaⅠ和Sau3A的酶切位点。 (3)标记有32p的同样DNA片段,用HhaⅠ完全酶切,进行电泳,那么用EB染色或放射自显影,会分别得到什么样的图?
由MNNG(亚硝基胍)引起的诱变损伤的本质以及它从DNA上被修复的机制可以用下面的实验来鉴定。为了确定诱变损伤的本质,未经处理的细菌和已用低剂量MNNG处理的细菌都在含50μg/ml的3H-MNNG的培养物中培养10min。分离它们的DNA并水解成核苷酸,然后经过纸层析分析放射性的嘌呤,结果如图Q12.2所示:

图Q12.2 层析法分离未被处理和已被低剂量MNNG处理的细菌DNA中被标记的甲基化嘌呤实线表示未被处理细菌DNA中的甲基化嘌呤;虚线表示MNNG处理的细菌所得结果
为了研究诱变损伤切除的机制,首先纯化负责切除的酶,把不同量的酶(相对分子质量19000)和已被3H标记含0.26pmol突变碱基的DNA一起温育,分析切除动力学。在不同时间取样,分析DNA以确定还存在多少突变残基(图Q12.3)。当在5℃而不是37℃时重复这个实验时,虽然最初的切除速率较慢,却得到一样的终点。

图Q12.3纯化的甲基转移酶把3H标记的甲基从DNA上切除所示为纯化酶的量
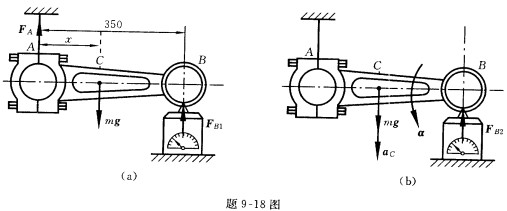
为确定题9—18图(a)所示质量m=4kg的连杆的转动惯量警察,将连杆一端用绳吊起,另一端放在台秤上,台秤测出的力F1=14.6N,当把绳断开的瞬时,台秤测出的力F2=9.37N;试求连杆对质心轴的转动惯量。
信号x(t)的最高频率为fx,若用下图所示的q(t)对x(t)进行自然抽样,试确定已抽样信号的频域表示式,并画出其频谱图(设Ts=5τ)。

利用一个包含纯化的RNA聚合酶的核心酶、DNA模板、σ因子以及标记核苷酸(32pppN)的系统,来研究σ因子在原核转录中的作用。在10-10mol和10-11mol两种不同浓度的核心酶催化下32P掺入到RNA的图如下所示,σ因子浓度恒定为10-12mol。

考虑下面血红蛋白α、β链协调合成的实验。家兔的网织红细胞被3H—Lys标记10min(标记时间相对一条珠蛋白单链的合成是足够的),然后离心分离带新生链的核糖体,除去可溶珠蛋白。新生珠蛋白链被胰蛋白酶消化,使肽链C端以Lys或Arg结尾,接着用HPLC(高效液相色谱)分离出这些肽并测定它们的放射性。图Q11.2为每条肽链中相对Lys残基的位置的放射性标志图。

图Q11.2 α-珠蛋白、β-珠蛋白的合成