 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
CoCl3.4NH3用H2SO4溶液处理再结晶,S042-可取代化合物中的Cr-,但NH3的含量不变。用过量AgNO3处理该
A.[Co(NH3)4]Cl3
B.[Co(NH3)4Cl]Cl2
C.[Co(NH3)4Cl2]Cl
D.[Co(NH3)4 Cl3]
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.[Co(NH3)4]Cl3
B.[Co(NH3)4Cl]Cl2
C.[Co(NH3)4Cl2]Cl
D.[Co(NH3)4 Cl3]
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“CoCl3.4NH3用H2SO4溶液处理再结晶,S042-可…”相关的问题
更多“CoCl3.4NH3用H2SO4溶液处理再结晶,S042-可…”相关的问题
完成并配平下列各反应的方程式: (a)用浓H2SO4焙烧法处理氟碳铈镧矿 (b)镧、铈、镨、铽草酸盐的高温分解 (c)Eu3+(aq)被锌汞齐还原 (d)标准Fe3+(aq)滴定Eu2+(aq) (e)标准Ce4+(aq)滴定Fe2+(aq) (f)酸性溶液中Ln3+与杂质离子Th4+和Fe3+的分离 (g)水溶液中Eu3+与其他Ln3+的分离 (h)水溶液中Ce3+与其他Ln3+的分离
有一黑色化合物(I),不溶于碱,加热时可溶于浓盐酸而放出气体(II)。将(I)与NaOH和KClO3共热,它就变成可溶于水的绿色化合物(III)。若将(III)酸化,则得到紫红色溶液(IV)和沉淀(I)。用Na2SO3溶液处理(IV)时,也可得到沉淀(I)。若用H2SO4酸化的Na2SO3溶液处理(Mn2+盐),则得到几近无色的溶液(V)。问(I), (II), (III), (IV)各为何物?
A(I) = MnO2, (II)= Cl2, (III)= MnO42-, (IV)= MnO4-;
B(I) = MnO2, (II)= Cl2, (III)= MnO4-, (IV)= MnO42-;
C(I) = MnO2, (II)= O2, (III)= MnO42-, (IV)= MnO4-;
D以上都不是
用库仑法测定溶液中的As(Ⅲ),电解质为0.1 mol·L-1的H2SO4和0.2 mol·L-1的KBr,在_______极上产生滴定剂,电极反应是________。
某病人血浆样品,用pH计测定溶液的pH=7.20。取5.00mL血浆加入1.000mL0.100mol·L-1的H2SO4,加热除去产生的CO2。然后用0.0200mol·L-1的NaOH溶液滴定,至终点时消耗NaOH的体积为3.600mL。请判断病人是否酸碱中毒及其原因。
根据实验测得1mol H2SO4溶于n1mol水中时,溶解热△isolH可用下式表示
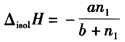 式中a=7.473×104J;b=1.798mol。试求: (1)积分溶解热,用1mol H2SO4溶于10mol水中。 (2)积分稀释热,在上述溶液中再加10mol水。
式中a=7.473×104J;b=1.798mol。试求: (1)积分溶解热,用1mol H2SO4溶于10mol水中。 (2)积分稀释热,在上述溶液中再加10mol水。
A、(I)=NaMnO4,(II)=O2,(III)=NaMnO3;
B、(I)=NaNO3,(II)=O2,(III)=NaNO2;
C、(I)=NaClO3,(II)=O2,(III)=NaClO;
D、(I)=NaSO4,(II)=O2,(III)=NaSO3
需要多少立方厘米浓度为0.1000mol·dm-3的H2SO4溶液,方能使下列碱溶液完全反应:
测定一工业H2SO4含量,取样量为1.1250g,稀释成250cm3,摇匀后移取25.00cm3,消耗0.1340mol·dm3NaOH溶液15.40cm3,求该工业硫酸中H2SO4的质量分数。