 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知某气体混合物的组成如下: 组分 甲烷 乙烷 丙烯 丙烷 异丁烷
已知某气体混合物的组成如下:
组分 | 甲烷 | 乙烷 | 丙烯 | 丙烷 | 异丁烷 | 正丁烷 | ∑ |
组成 | 0.05 | 0.35 | 0.15 | 0.20 | 0.10 | 0.15 | 1.00 |
当操作压力p=2.76MPa时,求此混合物的露点。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知某气体混合物的组成如下:
组分 | 甲烷 | 乙烷 | 丙烯 | 丙烷 | 异丁烷 | 正丁烷 | ∑ |
组成 | 0.05 | 0.35 | 0.15 | 0.20 | 0.10 | 0.15 | 1.00 |
当操作压力p=2.76MPa时,求此混合物的露点。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知某气体混合物的组成如下: 组分 甲烷 乙烷 丙烯 丙烷 …”相关的问题
更多“已知某气体混合物的组成如下: 组分 甲烷 乙烷 丙烯 丙烷 …”相关的问题
拟进行吸收分离的多组分气体混合物的组成(摩尔分数)如下:
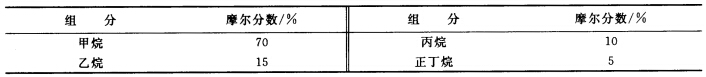 进料气在24℃,0.2026MPa压力下,在板式塔中用烃油吸收,烃油含1%正丁烷,99%不挥发性烃油,进塔的温度和压力与进料气相同。所用液气比为3.5。进料气中的丙烷至少有70%被吸收。甲烷在烃油中的溶解度可以忽略,而其它的组分均形成理想溶液。估算所需的理论级数和出口气相的组成。各组分有关物性数据如下:
进料气在24℃,0.2026MPa压力下,在板式塔中用烃油吸收,烃油含1%正丁烷,99%不挥发性烃油,进塔的温度和压力与进料气相同。所用液气比为3.5。进料气中的丙烷至少有70%被吸收。甲烷在烃油中的溶解度可以忽略,而其它的组分均形成理想溶液。估算所需的理论级数和出口气相的组成。各组分有关物性数据如下:
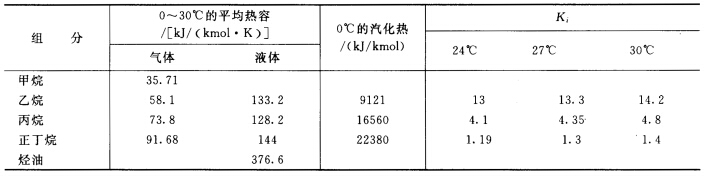
所需理论级数;
氧化偶氮苯在硫酸(质量分数为0.8822)的催化下转化为羟基偶氮苯,反应过程中定期从反应混合物中取出已知体积的样品,并立即用碱性乙醇溶液终止反应。产物羟基偶氮苯的浓度可通过样品溶液对一定波长(435nm)光的吸收来测定。在确定的波长下,只有产物对光有吸收。反应在298.15K下进行,测得不同反应时间样品吸光度IA的实验数据如下:
| t×103/s | 0.0 | 3.6 | 7.2 | 10.8 | 14.4 | 18.0 |
| IA | 0.007 | 0.134 | 0.250 | 0.343 | 0.416 | 0.476 |
| r×103/s | 21.6 | 27.0 | ∞ | |||
| IA | 0.529 | 0.590 | 0.781 |
已知反应物初始浓度cA0=1.87×10-3mol·dm-3,试确定该反应的级数和速率常数。(提示:若反映反应系统组成的某物理量L满足以下条件:1.具的加和性;2.与浓度成线性关系。则对于不可逆反应,系统组分A的浓度与物理量L满足下列关系式:
式中:L0,It,L∞分别表示0,t,∞时刻反应系统该物理量L的值,cA0,cA分别表示0,t时刻反应组分A的浓度值。)
某气体混合物由4种气体组成,在常压或低压下其粘度η与各组分的物质的量分数x1,x2,x3,x4之间有如下线性关系:
η=b0+b1x1+b2x2+b3x3+b4x4(1)
试根据下表所列实验数据确定方程中的各个系数,并计算其复相关系数。
| 各组分的物质的量分数 | 粘度η×102 | |||
| x1 | x2 | x3 | x4 | g·m-1·s-1 |
| 0.402 0.503 0.306 0.296 0.309 0.055 | 0.153 0.301 0. 109 0.365 0.405 0.153 | 0.053 0.133 0.224 0.009 0. 109 0.506 | 0.387 0.013 0.361 0.330 0.171 0.289 | 0.625 0.826 1.182 1.044 2.372 3.243 |
(提示:由于各组分摩尔分数之和等于1,故第4种气体的摩尔分数可以看成非独立变量,不必列入回归方程。)
已知373.15K时甲烷(1)一乙烷(2)一戊烷(3)混合物的virial系数如下(单位:cm3/mol),B11=一20,B22=一241,B33=一621,B12=一75,B13=一122,B23=一399,试用virial方程估算0.5MPa,373.15K时的等物质的量甲烷(1)一乙烷(2)-戊烷(3)混合物的摩尔体积(实验值5975cm3/mol)。
已知烃类混合物的组成如下表所列,用Chao-Seader法计算该混合物在638kPa压力下的泡点。
编号 | 1 | 2 | 3 | 4 | 5 | 6 | ∑ |
组分 | i-C_4^0 | n-C_4^0 | n-C_4^= | 反-2-C_4^= | 顺-2-C_4^= | C5 | |
摩尔分数 | 0.0023 | 0.0012 | 0.1437 | 0.3465 | 0.2763 | 0.2300 | 1.0000 |
在氧化铝为载体的镍催化剂上,进行苯气相加氧反应以生产环己烷,即
C6H6+3H2→C6H12
催化剂为圆柱状,直径和高度均为8mm,颗粒密度为0.9g/cm3,堆积密度为0.6g/cm3,反应混合物以质量速度为1500kg/(m3·h),通过反应器。已知在反应器的某一截面处,反应混合物组成为:C6H61.2%,H292%,环-C6H126.8%。气体温度为180℃,压力为0.10133MPa,反应速率为0.0195mol(环C2H12)/(g(cat)·h),试计算该处催化剂外表面的温度和苯浓度。
根据给定的温度、压力及混合气组成,可以估算出反应气体的物理性质如下:苯的扩散系数D=0.678cm2/s,气体混合物导热系数λg=0.7322kJ/(m·h·℃),混合气体黏度μ=1.161×10-5Pa·s,混合气体平均热容cp=37.24kJ/(kmol·℃),反应热(-△H)=213384J/mol
含有20%(体积)CO和80%(体积)N2的气体混合物通过FeO层使之还原为Fe,反应式如下:

假设反应能在1000K和1bar条件下达到平衡状态,计算每分钟能生成铁的量。已知Ka=0.52,气体混合物的流量为100mol·min-1。
颗粒外表面温度与浓度
在Al2O3为载体的Ni催化剂上进行苯气相加氢反应
C6H6+3H2→环-C6H12
催化剂为球形颗粒,直径为8mm,颗粒密度为0.9g/cm3,堆积密度为0.6g/cm3,反应物的质量流速为1500kg/(m2·h)。已知在反应器中某处反应物组成为1.2%C6H6,92%H2及6.8%环-C6H12气体温度为180℃,压力为0.10133MPa,反应速率为0.0195mol环-C6H12/(g(cat)·h)。试估算该处催化剂外表面温度及C6H6的浓度。
已知在给定温度、压力、混合气组成时气体的物理性质如下:
C6H6的扩散系数0.678cm2/s,气体混合物导热系数为0.7322kJ/(mol·℃),混合气体黏度为1.161×10-5Pa·s,混合气体平均热容为37.24kJ/(mol·℃),反应热为
(-△H)=213384J/mol。
A.t₁等于t₂
B.t₁小于t₂
C.t₁大于t₂
D.不确定
实验证实,某均相恒容反应的机理为由EB经H生成MA的两步连串反应:

已知:(1)每个阶段的反应物仅为一种物质;(2)第一步、第二步分别为零级和二级反应。
443K下,反应式各物质的液相组成如下:
| 反应时间 t/min | 液相组分(物质的量分数) | ||
| xH | xMA | xEB | |
| 0. 4.7 14.7 24.7 34.7 44.7 54.7 | 0 0.0170 0.0495 0.0802 0.1060 0.1265 0.1360 | 0 0.0005 0.0024 0.0120 0.0248 0.0515 0.0697 | 1.0000 0.9825 0.9481 0.9078 0.8692 0.8220 0.7942 |
试利用上述数据求出第一步和第二步的反应速率常数k1、k2。
(提示:可根据物质H的速率方程来求。)