 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某反应2A(s)+B(g)====2C(g)正反应的活化能为40kJ·mol-1,温度为1000K时 ,则该反应的
,则该反应的 和逆反应的活化能分别为( )。
和逆反应的活化能分别为( )。
A.-226kJ·mol-1和266kJ·mol-1
B.-226kJ·mol-1和274kJ·mol-1
C.-242kJ·mol-1和274kJ·mol-1
D.-242kJ·mol-1和282kJ·mol-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“某反应2A(s)+B(g)====2C(g)正反应的活化能为…”相关的问题
更多“某反应2A(s)+B(g)====2C(g)正反应的活化能为…”相关的问题
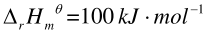 ,当反应达到平衡时,下列可以使反应向正向移动的措施是()。
,当反应达到平衡时,下列可以使反应向正向移动的措施是()。
















