 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
873K时电池Pb|PbCl2|Cl2(P氯气=l巴)的电动势为1.218V,计算电池反应的平衡常数。
873K时电池Pb|PbCl2|Cl2(P氯气=l巴)的电动势为1.218V,计算电池反应的平衡常数。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
873K时电池Pb|PbCl2|Cl2(P氯气=l巴)的电动势为1.218V,计算电池反应的平衡常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“873K时电池Pb|PbCl2|Cl2(P氯气=l巴)的电动…”相关的问题
更多“873K时电池Pb|PbCl2|Cl2(P氯气=l巴)的电动…”相关的问题
分别估算下列反应在873K时的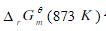 ,并比较Cu,Fe,Mn在873K时与O2结合能力的强弱。
,并比较Cu,Fe,Mn在873K时与O2结合能力的强弱。
目前正在研究的锌氯电池是一种可能成为电动汽车发动机能源的新型电池。该电池的电池反应如下所示:Zn(s)+Cl2(g)→ZnCl2(aq)。试求该电池电动势。
 CO(g)+H2O(g)在673K和873K时的标准平衡常数分别为8.0>(10—2和0.4),由此可知正向反应是吸热反应。()此题为判断题(对,错)。
CO(g)+H2O(g)在673K和873K时的标准平衡常数分别为8.0>(10—2和0.4),由此可知正向反应是吸热反应。()此题为判断题(对,错)。对原电池(-)Pb|Pb2+(c)||Cu2+(c)||Cu(),若往负极的电解质溶液中加入H2S,电池电动势______,原因是______;而往正极的电解质溶液中加入H2S,电池电动势______,原因是______。
若某原电池的一极发生的反应是: ,而另一极发生的反应为:
,而另一极发生的反应为: ,已测得φ(Cl2/Cl-)>φ(Fe3+/Fe2+),则该原电池的电池符号应为______。
,已测得φ(Cl2/Cl-)>φ(Fe3+/Fe2+),则该原电池的电池符号应为______。
12.根据硬软酸碱理论,判断下列化合物哪些易溶于水。
CaI2, CaF2, PbCl2,PbCl4, CuCN, ZnSO4
在1×10-3m3容器内应放入多少mol的PCl5才可得100mol的Cl2?已知反应 ,在250℃时的Kp=1.78。
,在250℃时的Kp=1.78。
采用电解NaCl水溶液制取氯气和烧碱时,如果阳极气体含有98.2%的Cl2和1.8%的O2,计算阳极反应的电流效率。