 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用重量法测定As2O3的含量时,将As2O3在碱性溶液中转变为 ,并沉淀为Ag3AsO4,随后在HNO3介质中转变为AgCl沉淀,并以AgCl称量。其化学因数为( )
,并沉淀为Ag3AsO4,随后在HNO3介质中转变为AgCl沉淀,并以AgCl称量。其化学因数为( )
A.As2O3/6AgCl
B.2As2O3/3AgCl
C.As2O3/AgCl
D.3AgCl/6As2O3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 ,并沉淀为Ag3AsO4,随后在HNO3介质中转变为AgCl沉淀,并以AgCl称量。其化学因数为( )
,并沉淀为Ag3AsO4,随后在HNO3介质中转变为AgCl沉淀,并以AgCl称量。其化学因数为( )A.As2O3/6AgCl
B.2As2O3/3AgCl
C.As2O3/AgCl
D.3AgCl/6As2O3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用重量法测定As2O3的含量时,将As2O3在碱性溶液中转变…”相关的问题
更多“用重量法测定As2O3的含量时,将As2O3在碱性溶液中转变…”相关的问题
某矿石样品0.5000克,用重量法测得样品中(Fe2O3+Al2O3)沉淀的总量为0.4230克,将沉淀溶解在酸性溶液中,用重铬酸钾氧化还原滴定法测定铁的含量,将Fe3+还原为Fe2+后,用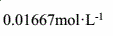 的重铬酸钾标准溶液滴定,用去35.00cm3,求此样品中Fe2O3与Al2O3的含量各为多少?(M(Fe)=55.847,M(Al)=26.982,M(O)=15.999。)
的重铬酸钾标准溶液滴定,用去35.00cm3,求此样品中Fe2O3与Al2O3的含量各为多少?(M(Fe)=55.847,M(Al)=26.982,M(O)=15.999。)
某矿石样品0.5000克,用重量法测得样品中(Fe2O3+Al2O3)沉淀的总量为0.3630克,将沉淀溶解在酸性溶液中,用重铬酸钾氧化还原滴定法测定铁的含量,将Fe2+还原为Fe2+后,用
用MgNH4PO4重量法测定某磷矿样中P2O5的含量。称取含水分0.93%的该矿样0.6124g,经一系列处理后得到0.3425g Mg2P2O7。求分别以干基和以湿基计算时,矿样中P2O5的质量分数。[M(P2O5)=141.99g·mol-1,M(Mg2P2O7)=222.55g·mol-1]
重量法测定白云石中钙的含量,已知其氧化钙含量在30%左右。称取0.2803g,加热溶解并趁热加入(NH4)2C2O4调节溶液的pH后,得到CaCO3沉淀。为了使洗涤时造成溶解损失的误差≤0.01%,应该用100mL多大浓度的(NH4)2C2O4作洗涤液(用质量体积百分数≤0.01%表示)?(CaC2O4的Ksp=2.3×10-9,Mr(CaO)=56.08,Mr((NH4)2C2O4)=124)
将某含As样品8.00g处理成As(亚)溶液后,置于电解池中,于弱碱性介质中在100mA的恒定电流下用电解产生的I2进行库仑滴定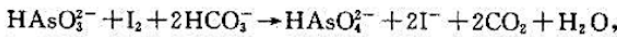 ,经15.0min到达滴定终点,试计算样品中As2O3的含量。已知,M(As2O3)=197.84g•mol^-1。
,经15.0min到达滴定终点,试计算样品中As2O3的含量。已知,M(As2O3)=197.84g•mol^-1。
A.加入的
C.沉淀完成后立即过滤 D.沉淀在热溶液中进行
用重量法测定试剂Na2HPO4·12H2O的纯度,首先是将试剂中的