 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
利用下述电池测pH。(-)Pt|H2(100kPa)|HCl(xmol·dm-3)||SCE()。试写出电池电动势与pH相关的方程式。若上述电池
利用下述电池测pH。(-)Pt|H2(100kPa)|HCl(xmol·dm-3)||SCE()。试写出电池电动势与pH相关的方程式。若上述电池电动势为0.444V,忽略液接电位,则此HCl溶液的pH为多少?[E(SCE)=0.2438V]
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
利用下述电池测pH。(-)Pt|H2(100kPa)|HCl(xmol·dm-3)||SCE()。试写出电池电动势与pH相关的方程式。若上述电池电动势为0.444V,忽略液接电位,则此HCl溶液的pH为多少?[E(SCE)=0.2438V]
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“利用下述电池测pH。(-)Pt|H2(100kPa)|HCl…”相关的问题
更多“利用下述电池测pH。(-)Pt|H2(100kPa)|HCl…”相关的问题
电池Mo(S)|MoS2(S)|H2S(100kPa)|KCl(0.01mol/kg)|HCl(0.01mol/kg)|H2(100kPa)|Pt,测得其在不同温度下的电池电动势数据为 T/K 288 298 308 E/V 0.4148 0.4119 0.4087 (1)写出电极反应和电池反应; (2)由题给数据推导出电池反应的平衡常数与温度的关系式,并计算△rHm; (3)用电化学方法计算298K时电池反应的△rSm,将其与热力学方法计算所得结果相比较可得出什么结论?298K时,物质的规定熵数据为 物质 H(g)H2S(g) Mo(s) MoS2(s) Sm/[J/(K.mol)] 130.6 205.6 28.58 62.59
双曲型动力学方程参数估值
在固体催化剂上进行气相反应
C6H5CH3(T)+H2(H)→C6H6(B)+CH4(M)
600℃等温下进行该反应,数据列于下表:
序号 | rT×1010mol/(g·s) | pT | pH | pB | pM | frac{p_{T}p_{H}}{r_{T}}times10^{-8} |
1 | 41.6 | 1 | 1 | 1 | 0 | 2.40 |
2 | 18.5 | 1 | 1 | 4 | 0 | 5.40 |
3 | 71 | 1 | 1 | 0 | 0 | 1.41 |
4 | 284 | 1 | 4 | 0 | 0 | 1.41 |
5 | 47 | 05 | 1 | 0 | 0 | 1.06 |
6 | 117 | 5 | 1 | 0 | 0 | 4.27 |
7 | 127 | 10 | 1 | 0 | 0 | 7.87 |
8 | 131 | 15 | 1 | 0 | 0 | 11.45 |
9 | 133 | 20 | 1 | 0 | 0 | 15.03 |
表中rT为甲苯转化速率,通过模型筛选,该反应动力学方程为
试计算600℃时的动力学参数k、KT、KB。
A . 消除温度的影响
B . 提高测定的灵敏度
C . 扣除待测电池电动势与试液pH值关系式中的“K”
D . 消除干扰离子的影响
A.p₁、p₂可任意取值
B.p₁>p₂
C.p₁=p₂
D.p₁<p₂
密度为ρ1=880kg/m3的原油流过如图所示的内径不变的弯管时,在弯管前、后1-1和2-2截面上装有水银测压计。测得水银柱高度差为h3=25cm,水银密度为ρ2=13600kg/m3,试求原油流过这段弯管的能量损失。已知h1=550mm,h2=750mm。

pH值为0时,
1/2O2+2H++2e→H2O,E0'=1.23V
该氧化还原反应在pH为0,还是pH为7的条件下更容易发生?利用电化学和化学平衡原理解释。
试证明平底梯形断面明渠中水跃前后水深满足下述关系
式中:β=b/(mh1);η=h2/h1;。
碘化氢的分解反应为
H2+I2-2HI=0,
实验测得该反应的平衡恒量K用下式表示
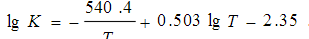 设在最初未发生分解时,除有N0mol的HI外,还同时有αN0mol的H2(这个问题称为有多余氢存在下HI的分解问题),又设I2不分解.试比较α=0与α=1两种情形在T=500K,1000K,1500K时的分解度
设在最初未发生分解时,除有N0mol的HI外,还同时有αN0mol的H2(这个问题称为有多余氢存在下HI的分解问题),又设I2不分解.试比较α=0与α=1两种情形在T=500K,1000K,1500K时的分解度
