 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知反应在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温
已知反应 在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。
在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应 在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。
在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应在1173K达到平衡时,测得平衡常数Kc=1.00。…”相关的问题
更多“已知反应在1173K达到平衡时,测得平衡常数Kc=1.00。…”相关的问题
A.向生成NO₂的方向进行
B.正好达到平衡
C.向生成N₂O₄的方向进行
D.难以判断其进行方向
工业锅炉进行热平衡测试时,按《工业锅炉热工性能试验规程(GB/T10180-2003)》规定()
A.测定锅炉效率应同时采用正平衡法和反平衡法
B.锅炉效率取正平衡法与反平衡法测得的平均值
C.锅炉效率以正平衡法测定值为准
D: 燃固体燃料正、反平衡效率之差不大于5%。
A.错误
B.正确
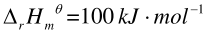 ,当反应达到平衡时,下列可以使反应向正向移动的措施是()。
,当反应达到平衡时,下列可以使反应向正向移动的措施是()。A.增加系统的温度
B.增加A物质的分压
C.增加C物质的分压
D.降低A物质的分压
A.正确
B.错误
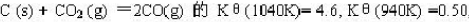 ,下列叙述中不正确的是()。
,下列叙述中不正确的是()。A.恒温、恒容条件下,压入氖气,化学平衡不移动
B.上述反应为放热反应
C.增大体系的总压,平衡发生移动
D.增大二氧化碳的浓度,平衡向正反应方向移动
把一种处于平衡态的N2(g),H2(g),NH3(g)的混合物从1.5 L烧瓶中移入5.00 L烧瓶中,当反应在趋于平衡的过程中,向哪个方向移动?
A.政府财政收支平衡
B.出现财政赤字
C.出现财政盈余
D.以上都不对