 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
6MPa、150℃的乙烷(C2H6)在换热器中冷却到50℃,进入换热器的容积流量为0.1m3/s,乙烷的平均定压比热为1.7662kJ/
6MPa、150℃的乙烷(C2H6)在换热器中冷却到50℃,进入换热器的容积流量为0.1m3/s,乙烷的平均定压比热为1.7662kJ/(kg·K),试求乙烷的放热量、熵变及熵产。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
6MPa、150℃的乙烷(C2H6)在换热器中冷却到50℃,进入换热器的容积流量为0.1m3/s,乙烷的平均定压比热为1.7662kJ/(kg·K),试求乙烷的放热量、熵变及熵产。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“6MPa、150℃的乙烷(C2H6)在换热器中冷却到50℃,…”相关的问题
更多“6MPa、150℃的乙烷(C2H6)在换热器中冷却到50℃,…”相关的问题
乙烷(C2H6)与丙烷(C3H8)的混合物,储于如图11-2所示的气缸中。活塞与重物的重量恰好能维持气缸内压力为3.5MPa,初态时活塞被挡块挡着,这时气缸容积为0.6m3,混合物的温度为30℃,压力为70kPa,乙烷的摩尔分数为0.20。有一乙烷的输气管道,管内乙烷的温度为30℃,压力为7MPa。管道通过阀门可与气缸连通。现打开阀门并卸去挡块,乙烷就充入气缸。当气缸内温度达到65℃,乙烷的摩尔分数为0.60时,才把阀门关闭。周围环境温度为30℃。

在25℃和1atm时乙烷在正庚醇中的溶解度为xE=0.0159。假设乙烷的活度系数模型为lnγE=B(1-xE)2,估计在25℃和20atm时下乙烷在正庚醇中的溶解度。已知乙烷的KE值如下,并假设正庚醇为近似于不挥发。
25℃和1atm:
25℃和20atm:
气相反应C2H6=C2H4+H2的标准平衡常数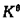 的表达式为:
的表达式为: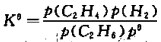 。()
。()
A.错误
B.正确
积分法处理动力学数据
在等温恒容间歇反应器中,进行二特丁基过氧化物的气相反应:
(CH3)3COOC(C2H3)3→C2H6+2CH3COCH3
简写为:
A→P+2S
实验用纯的二特丁基过氧化物,测得170℃时反应时间与系统总压的关系如下:
时间(min) 0.0 2.5 5.0 10.0 15.0 20.0
总压(mmHg) 7.5 10.5 12.5 15.8 17.9 19.4
试用积分法求该反应的级数和速率常数。
25℃和101.33kPa时乙烷(E)在正庚醇(H)中的溶解度是xE=0.0159,且液相的活度系数可以表示为
25℃和101.33kPa时乙烷(E)在正庚醇(H)中的溶解度是xE=0.0159,且液相的活度系数可以表示为lnγE=B(1一xE2),并已知25℃时的Henry常数:HE,H=27.0(在p=101.32kPa时);HE,H=162(在p=2026.4kPa时)。计算25℃、2026.4kPa时乙烷在正庚醇中的溶解度(可以认为正庚醇为不挥发组分)。
用PR方程计算甲烷(1)-乙烷(2)一丙烷(3)一正丁烷(4)一丙烯(5)等摩尔液体混合物在P=3MPa下的泡点温度和气相组成。
乙烷裂解生成乙烯: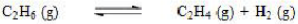 。在实际生产中常在恒温恒压下采用加入过量水蒸气的方法来提高乙烯的产率,这是因为随着水蒸气的加入,同时以相同倍数降低了p(C₂H₆)、p(C₂H₄)、p(H₂),使平衡向右移动。()
。在实际生产中常在恒温恒压下采用加入过量水蒸气的方法来提高乙烯的产率,这是因为随着水蒸气的加入,同时以相同倍数降低了p(C₂H₆)、p(C₂H₄)、p(H₂),使平衡向右移动。()
A.正确
B.错误