 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
0.5mol·L-1NH3·H2O(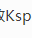 =1.8×10-5)溶液中加入NH4Cl固体,使c(NH4Cl)=0.2mol·L-1(忽略体积变化),此溶液的pH约为( )。
=1.8×10-5)溶液中加入NH4Cl固体,使c(NH4Cl)=0.2mol·L-1(忽略体积变化),此溶液的pH约为( )。
A.4.35
B.9.65
C.5.15
D.8.35
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
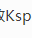 =1.8×10-5)溶液中加入NH4Cl固体,使c(NH4Cl)=0.2mol·L-1(忽略体积变化),此溶液的pH约为( )。
=1.8×10-5)溶液中加入NH4Cl固体,使c(NH4Cl)=0.2mol·L-1(忽略体积变化),此溶液的pH约为( )。A.4.35
B.9.65
C.5.15
D.8.35
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“0.5mol·L-1NH3·H2O(=1.8×10-5)溶液…”相关的问题
更多“0.5mol·L-1NH3·H2O(=1.8×10-5)溶液…”相关的问题
已知: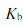 (NH3·H2O)=1.8×10-5,
(NH3·H2O)=1.8×10-5, (HAc)=1.8×10-5,按pH由大至小排列以下溶液(用序号排列)______。
(HAc)=1.8×10-5,按pH由大至小排列以下溶液(用序号排列)______。
①0.05mol·dm-3NH4Cl和0.05mol·L-1NH3·H2O混合液
②0.05mol·dm-3NaAc和0.05mol·L-1HAc混合液
③0.05mol·dm-3HAc
④0.05mol·dm-3NH3·H2O
⑤0.05mol·dm-3HCl溶液
⑥0.05mol·dm-3NaOH溶液
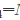 Na2SO4+S↓+SO2↑+H2O在室温下反应,以下4组溶液最先出现浑浊的是()
Na2SO4+S↓+SO2↑+H2O在室温下反应,以下4组溶液最先出现浑浊的是()A.0.1mol/LNa2S2O3和0.1mol/LH2SO4等体积混合
B.0.5 mol/LNa2S2O3和0.5mol/LH2SO4等体积混合
C.1mol/LNa2S2O3和1mol/LH2SO4等体积混合
D.0.5mol/LNa2S2O3和1mol/LH2SO4等体积混合
湿法炼锌过程中,假设由于电解液含铁太多,锌极表面有1%被铁覆盖,当锌极维持在-0.8V(vs SHE)时,估算锌沉积过程的电流效率。氢离子放电和金属锌沉积的阴极极化曲线如图所示,
(1)Zn|H2,0.5mol·L-1H2S04,20℃;
(2)Zn|Zn2+,0.5mol·L-1H2S04,20℃;
(3)Fe|H2,0.5mol·L-1,H2S04,20℃。

习题8.2
用极谱法分析测定某0.200 g试样中Zn2+的质量分数。在0.1mol?L-1NH3一NH4Cl溶液中加入0.05%的动物胶及0.5%Na2SO3除氧,测得试样的极限扩散电流为41.7uA。与试样作同样处理的标准zn2+的质量及波高如下。计算试样中zn2+的质量分数。

已知下列反应:
(1)2H2O2(1)→2H2O(1)+O2(g)
(2)H2O(1)→H2O(g)
求:(1)180gH2O2(l)分解的反应焓变△rHΘ?
(2)反应H2O2(l)→H2O(l)+1/2O2(g)的
(3)反应2H2O(l)+O2(g)→2H2O2(l)的
(4)反应H2O2(l)→H2O(g)+1/2O2(g)的
下述两反应哪一个反应过程中放出的热量较大?为什么? (a)A(g)+B(s)→C(1)+H2O(g) (b)A(g)+B(s)→C(1)+H2O(1)
下列各对物质中哪一个酸性较强?说明理由。
(1) EFe(H2O)6]3+和[Fe(H2O)62+
(2) [A1(H2O)6]3+和Ga(H2O)63+
(3) Si(OH)4和Ge(OH)4
(4) HClO3和HClO4
(5) H2CrO4和HMnO4
(6) H3PO4和H2SO4
配平下列反应方程式:
(1)____Cu+ ____HNO3(浓)=____Cu(N03)2+ NO2↑+ ____H2O
(2)____ Mn2++____S2O82-+____H20=____MnO4-+____SO42-+____H+
(3) ____Fe3++____H2S= ____Fe2++____S + ____H+
反应C(s)+H2O(g)=CO(g)+H2(g),为提高C(s)的转化率,可采取()措施。
A.增加C(s)的用量
B.增加H2O(g)的浓度
C.按1:1增加,C(s)和H2O(g)的用量
D.以上三种方法都可以
pH值为0时,
1/2O2+2H++2e→H2O,E0'=1.23V
该氧化还原反应在pH为0,还是pH为7的条件下更容易发生?利用电化学和化学平衡原理解释。
配平下列反应方程式:
(1)_____Na2S2O3+_____I2=_____Na2S4O6+_____NaI
(2)_____Cu+_____HNO3(稀)→_____Cu(NO3)2+_____NO↑+_____H2O
(3)_____KMnO4+_____H2C2O4+______H2SO4=_____MnSO4+_____CO2+_____K2SO4+_____H2O