 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于给定的T,p条件,假设二元系统的摩尔性质与组成的关系是M=x1M1+x2M2+Ax1x2。其中M1,M2分别为两纯组分的摩
对于给定的T,p条件,假设二元系统的摩尔性质与组成的关系是M=x1M1+x2M2+Ax1x2。其中M1,M2分别为两纯组分的摩尔性质,A是与组成无关的常数,求
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于给定的T,p条件,假设二元系统的摩尔性质与组成的关系是M=x1M1+x2M2+Ax1x2。其中M1,M2分别为两纯组分的摩尔性质,A是与组成无关的常数,求
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对于给定的T,p条件,假设二元系统的摩尔性质与组成的关系是M…”相关的问题
更多“对于给定的T,p条件,假设二元系统的摩尔性质与组成的关系是M…”相关的问题
二元系统的Wilson模型参数是λ12=1718cal·mol-1和λ21=166.6cal·mol-1,假设气相是理想气体,计算与x1=0.2,T=30℃的液相成平衡的气相组成和总压。已知


式中:a是平均增长率(标幺值);P是t年的需求量;P0是t0年的给定需求量。
假设某国1984年的电能需求峰值是480GW,平均增长率为3.4%。利用上述曲线和MATLAB以GW为单位,绘制从1984~1999年的预测电力负荷峰值需求图,并估计1999年的电能需求峰值。
A-B二元系固态在液态和固态均完全互溶(a相),并存在溶解度间隙。溶解度间隙的最高临界温度T<sub>c</sub>=800K。在550K以及B的摩尔分数x<sub>B</sub>=0.4时,自由能一成分曲线的二阶导数

二异丙醚脱水塔(见图3—2)进料F=15000kg/h,原料含水0.004(质量分数),饱和液体进料,塔压101.3kPa,
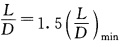 。要求产品乙二醇醚含水为0·0004(质量分数)。求
。要求产品乙二醇醚含水为0·0004(质量分数)。求
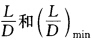 , 适宜进料位置和总平衡级数。假定恒摩尔流。恒沸数据:乙二醇醚(1)-水(2)yM=0.959,分层其上层x醚=0.994,下层x醚=0.012(质量分数),p=101.3kPa,T=62.2℃。假设相对挥发度为常数,从上述数据估计相对挥发度。
, 适宜进料位置和总平衡级数。假定恒摩尔流。恒沸数据:乙二醇醚(1)-水(2)yM=0.959,分层其上层x醚=0.994,下层x醚=0.012(质量分数),p=101.3kPa,T=62.2℃。假设相对挥发度为常数,从上述数据估计相对挥发度。
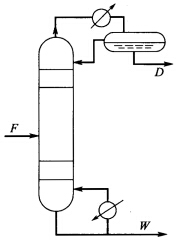
已知T=353.25K,p=101.325Pa,液体苯的摩尔体积为0.00009m3·mol-1,摩尔气化焓△Hvap=30780J·mol-1,蒸气压随温度的变化dp/dT=0.0003205Pa·K-1,试由此估算苯的viral系数。
理想气体物态方程是指p·V=n·R·T(n摩尔)。()
A.正确
B.错误
对于Namol的二元酸与Nbmol的二元醇生成聚酯的反应,设转化率为p时生成的水量为ωmol,试推导下列关系式:
对于一个处于热平衡态的均匀热力学系统,通常可选用体积V、质量M、密度ρ、压强p、温度T、内能U、熵S等等参量来加以描述,这些物理量不可能全部是独立变量,其中由系统内部分子热运动决定的量如p、T一定是独立变量。()
A.正确
B.错误