 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知某反应的<0,可知Ea(正)______Ea(逆),当温度升高时,v正______,v逆______,______,平衡向______移动。
已知某反应的

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知某反应的

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知某反应的<0,可知Ea(正)______Ea(逆),当温…”相关的问题
更多“已知某反应的<0,可知Ea(正)______Ea(逆),当温…”相关的问题
A.△rHmθ<0,△rSmθ>0
B.△rHmθ>0,△rSmθ<0
C.△rHmθ<0,△rSmθ<0
D.△rHmθ>0,△rSmθ>0
已知反应A(g)+2B(g)=2C(g)的△H>0,升高温度使v正增大,v逆减小,将导致平衡向右移动。( )
(X, )是可测空间,μ是(X,
)是可测空间,μ是(X, )上的有限实测度,A∈
)上的有限实测度,A∈ .若
.若 ,E
,E
 ,E
,E
存在正集A+和负集A-使 ,A+∪A-=X,且对
,A+∪A-=X,且对 ,有
,有
μ+(E)=μ(A+∩E),μ-(E)=-μ(A-∩E).
这里X的分解(A+,A-)称为μ的Hahn分解.
已知下列反应△rHΘm值的正、负,判断反应在高温和低温时的自发状态。 (1)2Fe(S)+3/2O2(g)=Fe2O3(s) △rHΘm<0 (2)2NH3(g)=N2(g)+3H2(g) △rHΘm>0 (3)C2H5OH(1)=C2H5OH(g) △rHΘm>0 (4)2Cl2(g)+7O2(g)=2Cl2O7(l) △rHΘm>0 (5)C2H5OH(l)+2O2(g)=2CO2(g)+3H2O(g) △rHΘm<0
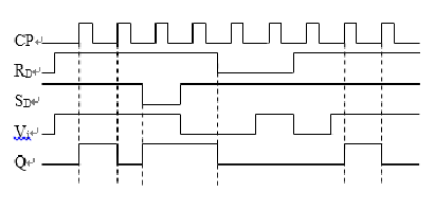
A.正边沿T触发器
B.负边沿D触发器
C.负边沿T触发器
D.正边沿D触发器
A.M2+不能发生歧化反应
B.M2+是强氧化剂
C.M是强还原剂
D.M4+ 与M 反应生成M2+
A.r= –0.84, b= 1.24
B.已知σy>σx ,计算得r= 0.62, b= 0 41
C.Lyx = 1.21 Syx = 1.21
D.r = 1.24 b = 3.5
E.Lxy = –124, r =0.98
化合物A参加的一级反应速率常数k为0.082 0min-1,已知初始浓度c(A)0=0.150 0 molL-1,使c(A)t=0.030 0 molL-1需用多长时间___________;