 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算298K时HI、H2、I2的标准热焓函数。已知HI、H2、I2的振动特征温度分别为3200K、6100K和610K。
计算298K时HI、H2、I2的标准热焓函数。已知HI、H2、I2的振动特征温度分别为3200K、6100K和610K。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算298K时HI、H2、I2的标准热焓函数。已知HI、H2、I2的振动特征温度分别为3200K、6100K和610K。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算298K时HI、H2、I2的标准热焓函数。已知HI、H2…”相关的问题
更多“计算298K时HI、H2、I2的标准热焓函数。已知HI、H2…”相关的问题
298K时,

(1)反应的
(2)当p(H2)=p(I2)=0.1kPa,p(HI)=0.010kPa时的
已知298K时的数据如下表:
物质 | H2(g) | I2(g) | HI(g) |
Delta_{f}G_{m}^{Theta }/(kJcdot mol^{-1}) | 0 | 19.359 | 1.7 |
求反应H2(g)+I2(g) 2HI(g)在298K时的
2HI(g)在298K时的。
2K时,反应H2(g)+l2(g)==2HI(g)的标准平衡常数为50.1。取5.3mol I2与7.94mol H2,使之发生反应,计算平衡时生成的HI的量。
试由下列数据求出298K下,Cu(s)、CuI(s)、HI(aq)及H2(


H2(g)和I2(g)在781K时发生如下反应:H2(g)+I2(g)→2HI(g)。已知HI的速率常数kHI为80.2dm3·mol-1·min-1,试求H2的速率常数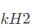 。
。
计算298.15K标准条件下反应2C2H5OH(1)→C4H6(g)+2H2O(g)+H2(g)的标准摩尔反应焓。已知298.15K时C2H5OH(1)、C4H6(g)和H2O(g)的标准摩尔生成焓分别为-235.10kJmol、-110.16kJ/mol和-241.82kJ/mol。
 的Kc=45.9,各物质以起始浓度c(H2)=0.0600mol·L-1、c(I2)=0.4000mol·L-1、c(HI)=2.00mol·L-1进行混合,在上述温度下,反应自发进行的方向是( )。
的Kc=45.9,各物质以起始浓度c(H2)=0.0600mol·L-1、c(I2)=0.4000mol·L-1、c(HI)=2.00mol·L-1进行混合,在上述温度下,反应自发进行的方向是( )。A.自发向右进行
B.自发向左进行
C.反应处于平衡状态
D.反应不发生
在298K和100kPa下,苯甲酸C6H5COOH(s)的标准燃烧热为-3226.87kJ· mol-1,C(石墨)和H2的标准燃烧热分别为-393.51kJ·mol-1和-285.83kJ·mol-1,求苯甲酸的标准生成热。
计算298K时,反应AgNO3(aq)+KCl(aq)→AgCl(aq)+KNO3(aq)的摩尔反应焓变。
在弹式量热计中燃烧氮化铌反应为
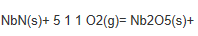
 在298K时测得热力学能的变化为-712.97kJ·mol-1,求此反应的焓变。
在298K时测得热力学能的变化为-712.97kJ·mol-1,求此反应的焓变。
卤素单质与H2化合的反应性随着F2,Cl2,Br2,I2的顺序依次减弱,因此形成的卤化氢的稳定性随HF,HCl,HBr,HI的顺序逐渐增加。( )