 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
正丙醇(1)与甲苯(2)所形成的共沸点是x1=0.6和T=92.6℃,P=760mmHg下形成,用van Laar方程估计两组成在系统温度
正丙醇(1)与甲苯(2)所形成的共沸点是x1=0.6和T=92.6℃,P=760mmHg下形成,用van Laar方程估计两组成在系统温度下的无限稀活度系数。已知两组分的饱和蒸气压是637.86mmHg和442.24mmHg。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
正丙醇(1)与甲苯(2)所形成的共沸点是x1=0.6和T=92.6℃,P=760mmHg下形成,用van Laar方程估计两组成在系统温度下的无限稀活度系数。已知两组分的饱和蒸气压是637.86mmHg和442.24mmHg。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“正丙醇(1)与甲苯(2)所形成的共沸点是x1=0.6和T=9…”相关的问题
更多“正丙醇(1)与甲苯(2)所形成的共沸点是x1=0.6和T=9…”相关的问题

(1)3-甲基-3-戊醇与H2SO4共热主要发生( )反应。
A.El B.SNl C.SN2 D.E2
(2)下列化合物沸点最高的是( )。
A.3-己醇 B.正己烷 C.2-甲基-2-戊醇 D.正庚醇
(1)3-甲基-3-戊醇与H2SO4共热主要发生( )反应。
A.El B.SNl C.SN2 D.E2
(1)下列化合物沸点最高的是( )。
A.3-己醇 B.正己烷 C.2-甲基-2-戊醇 D.正庚醇
证明(1)p-x1-y1图上泡点曲线的斜率为
 (2)若液相的超额吉氏函数模型是GE/RT=Bx1x2,则当
(2)若液相的超额吉氏函数模型是GE/RT=Bx1x2,则当
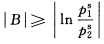 时有共沸点存在;且对于
时有共沸点存在;且对于
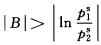 和B<2时,共沸组成是x1az=y1az=
和B<2时,共沸组成是x1az=y1az=
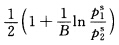
在101.325kPa下,1 kg水中溶有不挥发的0.2mol B和0.3mol C物质形成稀溶液,已知水(M=18.02g/mol)的沸点升高常数kb=0.52K.ks/mol。 (1)求该溶液的沸点; (2)水的摩尔气化热。
液体H2O(A),CCl4(B)的饱和蒸气压与温度的关系如表6-4所示。
表6-4
|
两液体成完全不互溶系统。
(1)绘出H2O-CCl4系统气、液、液三相平衡时气相中H2O,CCl4的蒸气分压对温度的关系曲线;
(2)从图中找出系统在外压101.325kPa下的共沸点;
(3)某组成为yB(含CCl4的摩尔分数)的H2O-CCl4气体混合物在101.325kPa下恒压冷却到80℃时,开始凝结出液体水,求此混合气体的组成;
(4)上述气体混合物继续冷却至70℃时,气相组成如何?
(5)上述气体混合物冷却到什么温度度时,CCl4也凝结成液体,此时气相组成如何?
二元系乙醇(1)-苯(2),在45℃,p=0.041MPa时形成共沸物,其共沸物组成为x1(共沸)=y1(共沸)=0.4。试求45℃,x1=0.616时的平衡压力p及y1。已知:45℃时,

用萃取精馏法分离正庚烷(1)-甲苯(2)二元混合物。原料组成z10.5;z20.50。采用苯酚为溶剂,要求塔级上溶剂浓度xS=0.55(摩尔分数);操作回流比为5和饱和蒸汽进料;平均操作压力为124.123kPa。要求馏出液中含甲苯不超过0.8%(摩尔分数),塔釜液含正庚烷不超过1%(摩尔分数)(以脱溶剂计),试求溶剂与进料比和理论级数。