 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一定温度下,反应CaCO3(s)CaO(s)+CO2(g)处于平衡状态,若将CaO的量加倍,下述陈述正确的是()
在一定温度下,反应CaCO3(s)
 CaO(s)+CO2(g)处于平衡状态,若将CaO的量加倍,下述陈述正确的是()。
CaO(s)+CO2(g)处于平衡状态,若将CaO的量加倍,下述陈述正确的是()。
A.反应商加倍
B.反应商减半
C.CaCO3的数量增加
D.CO2的分压不变
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一定温度下,反应CaCO3(s)
 CaO(s)+CO2(g)处于平衡状态,若将CaO的量加倍,下述陈述正确的是()。
CaO(s)+CO2(g)处于平衡状态,若将CaO的量加倍,下述陈述正确的是()。
A.反应商加倍
B.反应商减半
C.CaCO3的数量增加
D.CO2的分压不变
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在一定温度下,反应CaCO3(s)CaO(s)+CO2(g)…”相关的问题
更多“在一定温度下,反应CaCO3(s)CaO(s)+CO2(g)…”相关的问题
一定温度下,反应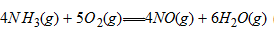 处于平衡态,若将CaO加倍,下列叙述正确的是
处于平衡态,若将CaO加倍,下列叙述正确的是
(A) 反应商加倍 (B) 反应商减半 (C) CaCO3量增加 (D) P(CO2)不变
反应CaCO3(s)→CaO(s)+CO2(g)的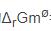 =179.2kJ·mol-1,故较高温度时,正反应可自发进行。
=179.2kJ·mol-1,故较高温度时,正反应可自发进行。
CaCO3(s)==CaO(s)+CO2(g)的标准平衡常数为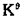 ,则CaCO3的分解压p=
,则CaCO3的分解压p=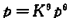 。()
。()
A.错误
B.正确
在一定温度和体积下,反应Sn(s)+2Cl2(g)
 SnCl4(g)达到平衡状态。已知正向反应是放热的,则采取的下列措施中,有利于增加SnCl4物质的量的是()。
SnCl4(g)达到平衡状态。已知正向反应是放热的,则采取的下列措施中,有利于增加SnCl4物质的量的是()。
A.升高温度
B.缩小体积
C.加入Sn(s)
D.通入N2
A.△rHmθ<0,△rSmθ>0
B.△rHmθ>0,△rSmθ<0
C.△rHmθ<0,△rSmθ<0
D.△rHmθ>0,△rSmθ>0
称取含CaCO3的石灰石试样(假设不含干扰物质)0.3000g,加入25.00mL0.2500mol·L-1HCl溶液,煮沸使反应完全。然后用0.2000mol·L-1NaOH溶液返滴定,用去5.84mL。求该石灰石中CaCO3的质量分数及用CaO表示分析结果的质量分数。已知M(CaCO3)=100.09g·mol-1,M(CaO)=56.08g·mol-1。
有一石灰石试样,假设其仅含CaCO3及其它不与酸作用的物质,现称取该试样0.3000g,加入25.00cm30.2500mol·dm3的HCl溶液,煮沸让它们反应完全,用0.2000mol·dm-3NaOH溶液返滴定,用去5.84cm3,求这种石灰石中CaCO3及CaO的质量分数。
9.有一石灰石试样,假设其仅含CaCO3及其它不与酸作用的物质,现称取该试样0.3000g,加入25.00cm30.2500mol·dm3的HCl溶液,煮沸让它们反应完全,用0.2000mol·dm-3NaOH溶液返滴定,用去5.84cm3,求这种石灰石中CaCO3及CaO的质量分数。
A.化学平衡状态是正逆反应都停止的状态;
B.反应N2(g)+O2(g)====2No(g)和

C.反应C(s)+CO2(g)====2CO(g),一定温度下达到平衡后,降低压力,正、逆反应速率都减慢,但平衡向右移动;
D.多步反应的总平衡常数为各步反应平衡常数之和。
A.CaC2O4·H2O→CaC2O4; B. CaC2O4→CaCO3;
C. CaC2O4→CaO; D. CaCO3→CaO。
 与
与 最接近的是( )
最接近的是( )A.CCl4(g)+2H2O(g)→CO2(g)+4HCl(g)
B.CaO(s)+CO2(g)→CaCO3(s)
C.Cu2+(aq)+Zn(s)→Cu(s)+Zn2+(aq)
D.Na(s)+H+(aq)+H2O(l)→Na+(aq)+