 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知CH4的生成热为-74.9kJ·mol-1,H的生成热为218kJ·mol-1,碳的升华热为717kJ·mol-1,试计算甲烷分子中C—H键
已知CH4的生成热为-74.9kJ·mol-1,H的生成热为218kJ·mol-1,碳的升华热为717kJ·mol-1,试计算甲烷分子中C—H键的键能。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知CH4的生成热为-74.9kJ·mol-1,H的生成热为218kJ·mol-1,碳的升华热为717kJ·mol-1,试计算甲烷分子中C—H键的键能。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知CH4的生成热为-74.9kJ·mol-1,H的生成热为…”相关的问题
更多“已知CH4的生成热为-74.9kJ·mol-1,H的生成热为…”相关的问题
已知NO(g)的生成热为90.25kJ·mol-1,N2分子中叁键的键能为941.69kJ·mol-1,O2分子中双键的键能为493.59 kJ·mol-1,求NO(g)中N—O键的键能。
写出由元素化合生成1molCH4(g)的化学方程式,由下列方程和293K时的

C(s)+O2(g)====CO2(g)
CH4(g)+2O2(g)====CO2(g)+2H2O(l)
写出由元素化合生成1 mol CH4(g)的化学方程式,由下列方程和293 K 时的△rHmθ值计算CH4的生成热。 H2(g)+
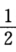 O2(g)→H2O(1) △rHmθ=一286.1 kJ.mol-1 C(s)+O2(g)→CO2(g) △rHmθ=一394.9 kJ.mol-1 CH4(g)+2O2(g)→CO2(g)+2H2O(1) △rHmθ=一882.0 kJ.mol-1
O2(g)→H2O(1) △rHmθ=一286.1 kJ.mol-1 C(s)+O2(g)→CO2(g) △rHmθ=一394.9 kJ.mol-1 CH4(g)+2O2(g)→CO2(g)+2H2O(1) △rHmθ=一882.0 kJ.mol-1
写出由元素化合生成1molCH4(g)的化学方程式,由下列方程式和298.15K时的
(1)H2(g)+1/2O2(g)====H2O(l)
(2)C(s)+O2(g)====CO2(g)
(3)CH4(g)+2O2(g)====CO2(g)+2H2O(l)

400K甲烷气CH4(g)与500K的空气在燃烧室内完全燃烧,过量空气系数α=1.5,生成物温度为1800K,试计算燃烧1mol甲烷燃烧室与外界传递的热量。已知CH4(g)的真实摩尔热容为
Cp,m=(14.16+75.55×10-3T-18.00×10-6T2)J/(mol·K)
设空气中N2与O2的物质的量之比为3.76:1,一些物质的标准生成焓如下:



另外,一些物质从298K到1800K或到550K的焓变分别为






已知
则MnO2的标准生成热
(A) 519.7; (B) -317.5; (C) -519.7; (D) 317.5。
已知25℃时:
| Delta _fH_m^{ominus }/(kJcdot mol^{-1}) | S_m^{ominus }/(Jcdot K^{-1}cdot mol^{-1}) | |
| H2O(l) H2O(g) | -285.8 -241.8 | 70.0 188.8 |
问25℃、标准状态下,水蒸发的过程是否为自发过程?如果不是,什么温度下可以自发。
 ②N2(g)+3H2(g)====2NH3(g)
②N2(g)+3H2(g)====2NH3(g) ③NH3(g)+HBr(g)====NH4Br(s)
③NH3(g)+HBr(g)====NH4Br(s) 则NH4Br(s)的标准摩尔生成热
则NH4Br(s)的标准摩尔生成热 =( )kJ/mol。
=( )kJ/mol。A.-270.83
B.270.83
C.-176.20
D.176.20