 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
欲标定0.2mol·dm-3NaOH溶液的标准浓度,预计消耗的NaOH溶液的体积在25cm3左右,若采用邻苯二甲酸氢钾作基准物
欲标定0.2mol·dm-3NaOH溶液的标准浓度,预计消耗的NaOH溶液的体积在25cm3左右,若采用邻苯二甲酸氢钾作基准物,应称取多少克?如改用草酸(H2C2O4·2H2O)作基准物,需称取多少克?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
欲标定0.2mol·dm-3NaOH溶液的标准浓度,预计消耗的NaOH溶液的体积在25cm3左右,若采用邻苯二甲酸氢钾作基准物,应称取多少克?如改用草酸(H2C2O4·2H2O)作基准物,需称取多少克?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“欲标定0.2mol·dm-3NaOH溶液的标准浓度,预计消耗…”相关的问题
更多“欲标定0.2mol·dm-3NaOH溶液的标准浓度,预计消耗…”相关的问题
欲标定NaOH溶液并已知天平的称量误差是±0.001g,请通过计算说明是用0.1000mol·L-1的二甲酸还是0.1000mol·L-1的邻苯二甲酸氢钾标定更好?
50mL0.20mol·dm-3Na2S溶液中,下列情况中[s2-]最大的是
(A) 加入50mL水 (B) 加入50mL0.20mol·dm-3NaOH (C) 加入S粉于溶液中
20cm3未知浓度的弱酸HA溶液,稀释至100cm3,以0.100mol·dm-3NaOH溶液进行电势滴定,所用电极为饱和甘汞-氢电极对,当一半酸被中和时,电动势读数为0.524V,滴定终点时电动势读数为0.749V,已知饱和甘汞电极的电势为0.2438V,求:
设天平称量误差为±0.2mg。现欲配制浓度均为0.01000mol·L-1的(coon)2及KHC8H4O4标准溶液各1L,用以标定NaOH溶液。计算需称取(COOH)2及KHC8H4O4质量的相对误差各为多少?计算结果说明什么?{M[(COOH)2]=90.038g·mol-1,M(KHC8H4O4)=204.22g·mol-1}
A.六亚甲基四胺加过量HCl的混合溶液
B.NaCl加入适量HCl的混合溶液
C.NaH2PO4与Na2HPO4的混合溶液
D.0.1mol·dm-3HAc与0.1mol·dm-3NaOH等体积混合
已知: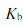 (NH3·H2O)=1.8×10-5,
(NH3·H2O)=1.8×10-5, (HAc)=1.8×10-5,按pH由大至小排列以下溶液(用序号排列)______。
(HAc)=1.8×10-5,按pH由大至小排列以下溶液(用序号排列)______。
①0.05mol·dm-3NH4Cl和0.05mol·L-1NH3·H2O混合液
②0.05mol·dm-3NaAc和0.05mol·L-1HAc混合液
③0.05mol·dm-3HAc
④0.05mol·dm-3NH3·H2O
⑤0.05mol·dm-3HCl溶液
⑥0.05mol·dm-3NaOH溶液
500ml 0.2mol/L NaCI溶液中含Na+
A.2.3g
B.2.93g
C.5.85g
D.7.1g
E.11.7g
9.有一石灰石试样,假设其仅含CaCO3及其它不与酸作用的物质,现称取该试样0.3000g,加入25.00cm30.2500mol·dm3的HCl溶液,煮沸让它们反应完全,用0.2000mol·dm-3NaOH溶液返滴定,用去5.84cm3,求这种石灰石中CaCO3及CaO的质量分数。
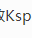 =1.8×10-5)溶液中加入NH4Cl固体,使c(NH4Cl)=0.2mol·L-1(忽略体积变化),此溶液的pH约为( )。
=1.8×10-5)溶液中加入NH4Cl固体,使c(NH4Cl)=0.2mol·L-1(忽略体积变化),此溶液的pH约为( )。A.4.35
B.9.65
C.5.15
D.8.35