 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某压力下二组分沸点组成图中,处于最高或最低恒沸点时其自由度为零。()
A.错误
B.正确
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.错误
B.正确
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某压力下二组分沸点组成图中,处于最高或最低恒沸点时其自由度为…”相关的问题
更多“某压力下二组分沸点组成图中,处于最高或最低恒沸点时其自由度为…”相关的问题
由A-B组成的二元汽液平衡系统,若汽相为理想气体,液相活度系数模型符合对称归一化条件,其超额Gibbs函数符合GE/RT=βxAxB,β是温度的函数,测得80℃时二组分的无限稀释活度系数是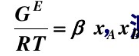 ,两纯组分的蒸气压为
,两纯组分的蒸气压为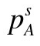 =120kPa,
=120kPa,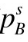 =80kPa,试问该系统在80℃时是否存在共沸点?若有,计算共沸点组成和压力。
=80kPa,试问该系统在80℃时是否存在共沸点?若有,计算共沸点组成和压力。
A、错误
B、正确
随着构成恒沸物的各组分的纯组分的蒸气压差的增大,恒沸组成变化规律为()。
A.向含低沸点组分多的浓度区移动
B.最低恒沸物向含低沸点组分多的浓度区移动,最高恒沸物向含高沸点组分多的浓度区移动
C.向含高沸点组分多的浓度区移动
D.最高恒沸物向含低沸点组分多的浓度区移动,最低恒沸物向含高沸点组分多的浓度区移动
随着构成恒沸物的各组分的纯组分的蒸气压差的增大,恒沸组成变化规律为( )。
a.向含低沸点组分多的浓度区移动;
b.最低恒沸物向含低沸点组分多的浓度区移动,最高恒沸物向含高沸点组分多的浓度区移动;
c.向含高沸点组分多的浓度区移动;
d.最高恒沸物向含低沸点组分多的浓度区移动,最低恒沸物向含高沸点组分多的浓度区移动。
A.二元理想溶液的压力组成图中,总压和各组分的分压与液相组成都成直线关系
B.完全互溶的二元物系,不形成恒沸物的非理想溶液的蒸汽总压都介于两纯组分蒸汽压之间
C.完全互溶的二元物系,由相律可知恒沸物在两相平衡时其自由度为“0”
D.完全不互溶的二元物系,当处于平衡状态时总压等于两饱和蒸汽压之和
在25℃时,二元系统处于气液液三相平衡状态,通过分析两个平衡的液相的组成得

(1) 两组分的活度系数;
(2) 平衡压力;
(3) 平衡气相组成。
正丙醇(1)与甲苯(2)所形成的共沸点是x1=0.6和T=92.6℃,P=760mmHg下形成,用van Laar方程估计两组成在系统温度下的无限稀活度系数。已知两组分的饱和蒸气压是637.86mmHg和442.24mmHg。
组分A按下列反应发生分解:
A====B+C
该反应是在60℃下于液相中进行的。反应的平衡常数为2。组分A、B和C在60℃下的饱和蒸气压分别为607.95kPa、1013.25kPa和810.60kPa。液体A和液体C形成理想溶液。液体B与由(A+C)组成的溶液中互不相溶。假设其汽相为理想气体。试计算该系统在60℃下的汽相组成和平衡压力。
通用气体常数R=1.987cal·mol-1·K-1或8.315J·mol-1·K-1(1cal=4.184J)。